人类的嵌合细胞恢复杜氏肌萎缩症至关重要的蛋白质
细胞由一个正常的人类肌肉细胞和肌肉细胞融合与杜氏肌萎缩症——一个人罕见但致命的肌肉dystrophy-were能够显著改善肌肉功能当植入肌肉疾病的小鼠模型。研究结果报道芝加哥伊利诺伊大学的研究人员干细胞审查和报告。
这些细胞名为“嵌合细胞”,是由结合一个正常的供体细胞包含一个功能基因的副本dystrophin-a结构性的肌肉蛋白质缺乏人与杜氏肌dystrophy-with细胞从接受者的疾病。2018年1月发表的一篇论文中干细胞的评论和报道,研究人员用老鼠的供体和受体细胞的嵌合细胞,增强抗肌萎缩蛋白水平37%,改善肌肉功能植入的肌肉小鼠模型杜氏肌萎缩症。新的细胞供体和受体的特征和与周围环境互动正常细胞。嵌合细胞产生抗肌萎缩蛋白仍然可行,30天。
领导的研究小组,Maria Siemionow,芝加哥大学医学院整形外科教授,报告使用类似的发现人类细胞杜氏肌萎缩症的小鼠模型中植入。
“我们的研究结果指出,这些细胞的长期生存并帮助建立嵌合细胞作为小说的使用有前途的潜在治疗杜氏肌萎缩症患者,“面部。她的团队期待人类临床试验在不久的将来,她说。
杜氏肌萎缩症是x染色体遗传障碍表现为渐进式肌肉变性和弱点,影响大约4000年新生男婴。
患者没有肌营养不良蛋白的基因,一种结构蛋白,有助于保持肌肉细胞完好无损。症状出现在儿童早期,通常3和5岁之间。运动机能的失调会导致肌肉无力和损失,最终导致呼吸或心脏衰竭和死亡。杜氏肌萎缩症治疗的进步,很多住在青少年和20多岁和30多岁,但目前还没有治疗这种疾病的方法。
有前途的治疗方法包括基因疗法干细胞疗法,但每个人都有缺点。基因治疗依赖于提供良好的副本缺失或功能失调的基因通过病毒细胞。不仅可以成为病毒感染的免疫细胞,治疗无效的渲染,但这也不能保证病毒只感染目标细胞。干细胞疗法,包含抗肌萎缩蛋白基因的细胞植入受体,要求收件人服用免疫抑制药物,预防产生排异现象。
“这不是传统的干细胞疗法”,面部说,论文的主要作者。“我们恢复肌营养不良蛋白这样接收者不需要服用抗排斥治疗,因为植入嵌合细胞可以逃避接受者的免疫系统。在传统的干细胞疗法中,“其他”植入细胞100%,抗排斥药物是必要的,以防止宿主免疫系统摧毁这些外来细胞。”
相比之下,嵌合细胞50%“自我”——许多生化和遗传特性的公民、这样可以诱骗接受者的免疫系统忽视他们。
“嵌合细胞足够的喜欢接受者自身的细胞,他们的免疫系统给了他们一个“通过”,“面部。
如果这些细胞被用来治疗杜氏肌萎缩症患者,然后正常肌肉细胞从收件人的父亲或近亲融合病人的肌肉细胞。
研究人员从杜氏肌萎缩症患者肌肉细胞融合肌肉细胞从正常、健康的捐赠者。
在实验室里,嵌合细胞被认为表达抗肌萎缩蛋白。
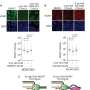
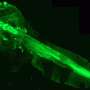
当细胞植入小鼠模型的腿部肌肉的杜氏肌肉营养不良症,肌营养不良蛋白水平上升大约20%的肌肉纤维的影响植入细胞post-implantation 90天,“足以产生肌肉功能显著改善,”克丽丝Siemionow说,整形外科副教授在芝加哥大学医学院和研究报告的合著者。
改进的被认为在60%以上肌肉功能植入老鼠的测试和改进测试超过20%的肌肉疲劳宽容。
玛丽亚和克丽丝面部,母亲和儿子,最近推出了一个公司来开发他们的嵌合细胞到一个治疗杜氏肌萎缩症治疗称为Dystrogen疗法。
更多信息:Maria Siemionow et al,肌营养不良蛋白表达嵌合(DEC)人类细胞提供了一个潜在的治疗杜氏肌肉营养不良症,干细胞的评论和报道(2018)。DOI: 10.1007 / s12015 - 018 - 9807 - z