重新利用现有的fda批准的抑制剂可能为卵巢癌提供新的治疗方法

Wistar的研究人员已经找到了重新利用一类被称为HDAC抑制剂的抗肿瘤化合物的基本原理,这种化合物已经被FDA批准用于治疗白血病等疾病,作为一种新的治疗ARID1A基因突变卵巢癌的选择。研究结果发表于细胞的报道.
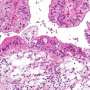
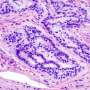
卵巢癌是最致命的妇科恶性肿瘤,而透明细胞亚型尤其因对常规化疗反应不佳而臭名昭著,给这些患者留下了有限的治疗选择。ARID1A基因在50%以上的卵巢透明细胞癌病例中发生突变。在正常细胞, ARID1A调节一组的表达基因通过影响染色质的结构,染色质是DNA和蛋白质的复合物,DNA包裹在我们的细胞中。ARID1A突变导致该蛋白或其功能的丧失,从而导致细胞的恶性转化。
在这项研究中,首席研究员Rugang Zhang博士和他的同事发现arid1a突变的卵巢癌对另一种染色质重塑酶HDAC2的抑制有选择性地敏感。这一发现与HDAC2高表达与这类癌症的不良预后相关的事实相一致。
“HDAC2和相关酶是很好的治疗靶点,许多HDAC抑制剂已经获得了FDA的批准,用于治疗造血恶性肿瘤,”张说,他是Wistar研究所癌症中心的副主任,同时也是基因表达和调控项目的教授和合作项目负责人。“我们认为,这些抑制剂可能被用于靶向arid1a突变卵巢癌。”
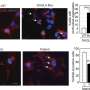
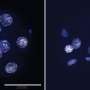
Zhang实验室发现,HDAC2抑制通过促进PIK3IP1基因的表达,抑制ARID1A失活细胞的增殖,诱导细胞程序性死亡。PIK3IP1是一种肿瘤抑制蛋白,作为促进细胞增殖和存活的重要信号轴的抑制剂。通过基因敲除方法和基因组学实验,研究人员确定,在ARID1A缺失的情况下,HDAC2结合PIK3IP1基因的调控元件并抑制其表达。因此,PIK3IP1的缺失允许肿瘤生长和扩散,而使用HDAC2抑制剂治疗可以恢复PIK3IP1的表达并阻止肿瘤的发展。
该团队探索了fda批准的HDAC抑制剂的使用,并证实了该治疗在arid1a失活卵巢癌小鼠模型中的治疗潜力。根据他们的观察,这种抑制剂减缓了肿瘤生长和荷瘤小鼠腹部液体的异常积聚,并提高了存活率。
“我们之前已经报道了另一种染色质重塑因子EZH2在arid1a突变卵巢中的作用癌症与PIK3IP1表达的拮抗调控机制类似,”该研究的第一作者、张实验室的博士后研究员Takeshi Fukumoto博士说。“然而,同时抑制EZH2和HDAC2可能是有利的,以阻止对单独任一抑制剂的耐药性发展。”
考虑到突变和损失表达式ARID1A基因在多种人类癌症中显著存在,新的发现可能对更广泛的恶性肿瘤的治疗有更广泛的意义。
进一步探索