科学家们解决阿尔茨海默病的遗传风险因素在人类脑细胞
用人类的脑细胞,格莱斯顿研究所的科学家们发现了起火的原因乃至一个潜在的解决方案——主要阿尔茨海默病的遗传风险因素,apoE4基因。
有apoE4基因的一个副本双打多一个人的发展中阿尔茨海默氏症的可能性疾病,有两份基因增加了12倍,风险是最常见的版本的基因相比,apoE3。
apoE4基因产生的蛋白质相同的名字。apoE4蛋白不同于apoE3蛋白质在只有一个点,但这一改变就足以改变其主要结构,因此,它的功能。科学家们一直不清楚为什么apoE4更损害大脑细胞比其他版本的蛋白质。
在一项新的研究发表在自然医学,研究人员揭示出apoE4赋予它在人类大脑细胞阿尔茨海默氏症的风险。更重要的是,他们能够消除造成的损害apoE4通过改变它,小分子,变成无害的apoE3-like版本。
一个更好的模式
大多数阿尔茨海默氏症研究药物开发是在疾病的小鼠模型。然而,一个接一个的临床试验的失败促使科学家们转向其他模型。
“阿尔茨海默病药物开发已基本失望在过去10年,”第一作者Yadong Huang说,医学博士,博士学位,高级调查员和格莱斯顿转化发展中心的主任。“许多药物工作漂亮在老鼠模型中,但是,到目前为止,他们已经在临床试验都失败了。领域内的一个问题如何差这些小鼠模型模拟人类疾病。”
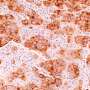
相反,黄决定使用人类细胞疾病模型和测试新药。由于诱导多功能干细胞技术,他的团队就能检查,第一次apoE4对人类大脑细胞的影响。要做到这一点,研究人员创建神经元从皮肤细胞捐赠的阿尔茨海默氏症患者有apoE4基因的两个副本,以及健康个体apoE3基因的两个副本。
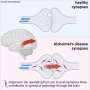
研究人员证实,在人类神经元,畸形apoE4蛋白质不能正常工作,分为致病细胞碎片。这个过程导致了许多问题通常存在于阿尔茨海默病,包括tau蛋白的积累和淀粉样蛋白肽。
值得注意的是,apoE4的存在不会改变的生产β淀粉样蛋白在小鼠神经元。但在人类细胞,科学家们注意到apoE4有一个很清晰的影响增加β淀粉样蛋白产量,这突显出物种差异apoE4控制淀粉样β蛋白代谢的方式。
“有一个重要的物种差异apoE4对β淀粉样蛋白的影响,“Chengzhong Wang说,博士论文的第一作者、前研究员格莱斯顿。“β淀粉样蛋白产量的增加是没有看到在老鼠神经元和之间的差异可以解释一些老鼠和人类对药物疗效。这将是未来药物发展的非常重要的信息。”
修复一个有毒蛋白质
一旦科学家证实apoE4确实,导致人体细胞损伤与阿尔茨海默氏症有关,一个关键的问题仍然存在:如何apoE4的存在导致细胞损伤吗?是apoE4的存在导致正常apoE3功能的丧失,或添加apoE4引起毒性作用吗?
“从根本上解决这个问题很重要,因为它改变你如何对待这个问题,”黄解释道,同时也是加州大学旧金山分校的神经学和病理学教授。“如果损坏所引起损失的蛋白质的功能,你想增加蛋白质含量来补充这些功能。但如果蛋白质的积累会导致有毒的功能,你想降低生产的蛋白质来阻止其不利影响。”
要回答这个问题,研究人员检查了脑细胞,没有产生形式的载脂蛋白e蛋白,细胞和神经元和运作就像apoE3。然而,如果研究人员添加apoE4,细胞变得充满病态与阿尔茨海默氏症有关。这一发现表明,apoE4-and的存在不是没有apoE3-promotes疾病。
最后,研究者寻找方法来修复apoE4造成的异常。在前期的工作中,黄和他的同事开发了一个类的化合物,可以改变结构的有害所以它像无害的apoE3 apoE4蛋白质蛋白质apoE4”结构,称为校正”。
治疗人类apoE4神经元结构校正器消除了阿尔茨海默氏症的迹象,恢复正常功能细胞,改善细胞的生存。黄和他的合作者在学术界目前正在和制药业提高化合物所以他们在未来可以在人类患者进行测试。
更多信息:获得的有毒载脂蛋白E4影响人类iPSC-derived神经元是由小分子结构改善校正器,自然医学(2018)doi: 10.1038 / s41591 - 018 - 0004 - z