双管齐下的方法可以抑制肺癌的病例数
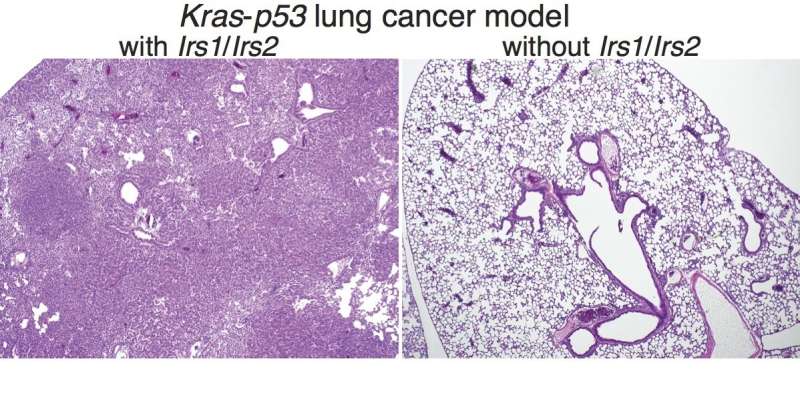
非小细胞肺癌,最常见的一种肺癌是癌症死亡的主要原因在美国一项新的研究表明,大约在4例,那些由喀斯特致癌基因,可成功治疗临床药物的组合已经可用。波士顿儿童医院的研究发表在今天的美国国家科学院院刊》上(PNAS)。
超过三十年,科学家们尝试,但收效甚微,目标KRAS基因突变致癌基因与药物。所以,一些研究人员试图目标相关的生物学途径。
这样一个途径包括胰岛素和胰岛素样生长因子- 1 (igf - 1),影响营养物质的吸收和释放,最终细胞生长。但这个途径尚未明确证明KRAS-driven燃料肺迄今为止,癌症,和抑制剂的igf - 1信号失败的临床试验中。事实上,最近对老鼠的研究其实看到肺肿瘤变得更加咄咄逼人。然而,本研究针对胰岛素/ igf - 1信号只是部分。
在新的研究中,研究人员利用基因技术完全阻断胰岛素/ igf - 1信号,提供最好的测试支持,但在KRAS-driven学习途径的作用肺癌。模型建立,完全挡住了通道可以减缓肿瘤增长还演示了第二步需要完全抑制。
“我们的研究使用了一个健壮的方式阻止胰岛素/ igf - 1信号和地址在KRAS-mutant肺一个长期存在的问题癌症Nada Kalaany说:“博士,研究员在波士顿儿童医院内分泌学和部门的资深作者的论文。“当你使用遗传学,结果可以更加确凿。”
一个新的模型在肺癌生长因子的影响
Kalaany的团队创造了一个新模型跨越两个品系的老鼠:一个模型的应变KRAS-driven肺癌,和另一个压力,缺乏胰岛素/ igf - 1信号,以前由莫里斯白色,博士,波士顿的儿童研究糖尿病。第二个模型删除两个关键基因,称为Irs1 Irs2,编码所谓“适配器”必需的蛋白质,胰岛素/ igf - 1信号(发现在1980年代由白色)。
新的,改良小鼠提供最好的模型为研究胰岛素/ igf - 1在肺癌的信号。研究人员表明,当了Irs1和Irs2都删除在肺部,胰岛素/ igf - 1信号消除和肺肿瘤强烈抑制。
“几乎所有的动物在这个肺癌模型通常在15周的喀斯特激活死去,”Kalaany说,他也是哈佛医学院助理教授和副教授的成员广泛的麻省理工学院和哈佛大学。“但是那些失去了Irs1和Irs2完全我们看到几乎没有在10到15周肿瘤。”
阻断肿瘤的解决方法
Kalaany和她的同事被这个结果感到兴奋,因为igf - 1抑制剂药物阻断胰岛素/ igf - 1信号有效Irs1/2删除已经可用。但他们也知道肿瘤细胞常常找出解决方法。
“我们决定让动物活得更长,果然,在16周左右我们开始看到一些肿瘤,“Kalaany说。”然后我们问道,这些肿瘤细胞如何能够克服Irs1和Irs2 ?”
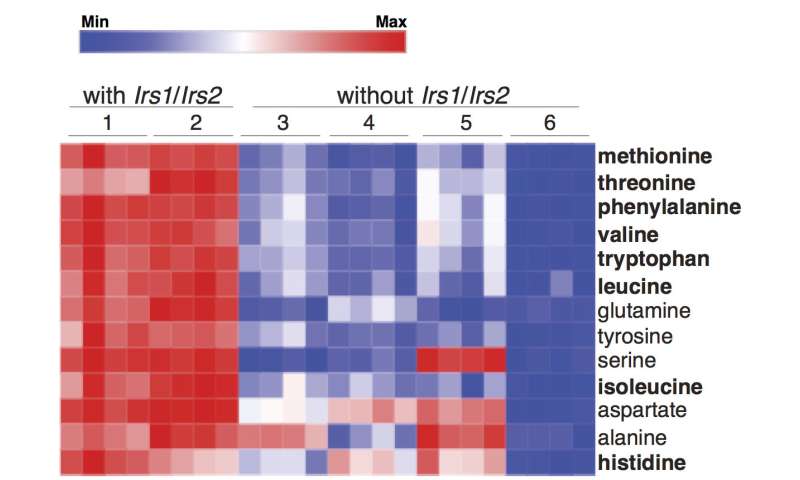
代谢分析显示,肿瘤细胞缺乏Irs1/2明显低水平的必需氨基酸,蛋白质的基石。然而,在细胞外,丰富的氨基酸。研究人员发现抑制时一样的胰岛素在人类肺癌/ igf - 1信号。
“生长因子igf - 1告诉细胞营养,所以当你压抑自己的信号时,肿瘤细胞的氨基酸和不觉得饥饿,“Kalaany解释道。“但是我们发现肿瘤细胞可以弥补这一生成和分解自己的蛋白质氨基酸。"
代谢途径癌症
原来还可以抑制蛋白质分解与现有的药物,如氯喹,它抑制自噬(字面意思是“自食”)和使用在一些抗癌药物试验,和bortezomib (Velcade),所谓的蛋白酶体抑制剂,用于治疗多发性骨髓瘤。
当Kalaany的团队注入了人类肿瘤细胞缺乏Irs1/2成老鼠,肿瘤没有增长。当他们添加抑制剂的蛋白质分解,增长几乎完全抑制。
尽管这两种类型的药物,以及igf - 1抑制剂,耐受性良好,需要注意在任何联合治疗,以避免毒性剂量,Kalaany说。这种疗法可能还更安全,如果针对肺部,她补充道。
就像另一个最近的研究从Kalaany对胰腺癌的实验室,目前的研究表明,针对癌症细胞代谢可以成为有效的武器。
“我们的工作试图识别肿瘤代谢相关性和漏洞,“Kalaany说。“如果我们确定合作,我们希望有一个临床试验非小细胞肺癌igf - 1抑制剂与自噬抑制剂或蛋白酶体抑制剂相结合。”
进一步探索















用户评论