新的证据揭示了帕金森病如何发生

德克萨斯州贝勒医学院的研究人员和儿童医院发现了意想不到的新发展的关键球员帕金森病的早期发病形式称为震颤麻痹。这些关键球员是天然保湿因子,一个家庭在细胞膜脂质分子的发现。研究人员提出,神经酰胺的关键连接之前确定独立细胞和基因缺陷与帕金森病有关,建议一种机制,可能导致的条件。研究结果,发表在《华尔街日报》细胞代谢,可能导致新的策略来预防或治疗的条件。
“许多基因与帕金森病或Parkinson-like疾病有关;尽管如此,仍然有小的了解这些基因导致这些条件,”博士说通讯作者雨果犬吠,分子和人类遗传学和神经科学教授贝勒医学院和霍华德休斯医学研究所的一位研究员。“在这项工作中,我们已经确定了新的贡献者的疾病我们建议可以提供一个联系以前无关基因这些疾病和细胞中观察到的缺陷。”
“当我加入了犬吠博士的实验室,我决定人类PLA2GA6基因。这个基因的突变引起神经退行性疾病,包括帕金森症”,第一作者说广林博士,博士后在分子和人类遗传学贝勒。“PLA2G6基因编码一种磷脂酶,一种修改的一种脂肪的酶称为磷脂。磷脂是神经系统的主要构件,但他们没有很透彻了。我们认为我们应该调查这磷脂酶在这些疾病。”
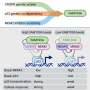
林和他的同事们开发了一种果蝇模型的人类状况的飞相当于人类PLA2GA6基因,叫做iPLA2-VIA,研究者确定表达在神经元和其他类型的细胞。这些突变体果蝇生活在大约三分之一的正常果蝇的寿命,提出了与人类细胞特征所观察到的类似PLA2G6突变基因。
“确认先前的结果由其他研究人员,我们也观察到,没有iPLA2-VIA基因果蝇是健康的年轻时,与年龄相关性神经退化,”林说。
此外,研究人员首次在突变的影响另外两个测量:爆炸敏感性和视觉系统的运作。爆炸敏感性是指响应果蝇的机械应力。他们观察到,尽管正常果蝇没有爆炸敏感性,这意味着他们立即恢复的影响,缺少iPLA2-VIA果蝇基因需要更长的时间来恢复;他们瘫痪后一段时间的影响,表明他们的神经系统的问题。
确定视觉系统的工作原理,研究人员进行了视网膜电流图测量的电响应光感受器,光感觉神经元,在不同时间的眼睛在成人果蝇的寿命。他们发现变异果蝇脑电活动的逐步丧失,结果再次显示在这些果蝇的神经系统缺陷。
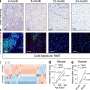
“我们进一步进行电镜研究仔细看看神经元的结构。我们发现在生病的苍蝇,感光细胞有许多夹杂物,把相似的结构,膜,这是一种症状,是错误的。正常细胞的内含物缺席,“犬吠说,他也是一个成员的简和丹邓肯神经研究所德克萨斯儿童医院。“我们还发现大部分线粒体结构畸形,这通常是帕金森氏症的一个特征,以及戏剧性的溶酶体增大,胞内结构参与膜和其它细胞成分的回收。总之,这些结果表明,iPLA2-VIA基因是重要的保持适当的膜结构和形状。”
一个令人惊讶的发现
“因为飞iPLA2-VIA基因编码一个磷脂酶,磷脂酶,修改,我们预期,苍蝇缺乏iPLA2-VIA基因磷脂的变化,提供了一个与我们观察到的结构和功能缺陷的苍蝇,“犬吠说。“令人惊讶的是,我们的分析表明,磷脂是正常的。我们没有预料到这个。”
然后,异常是什么?
研究人员观察了许多类型的脂质,发现大量的几乎所有重要的ceramides-lipids膜结构和函数增加果蝇缺乏iPLA2-VIA基因。这表明基因发挥作用的途径产生神经酰胺。
“我们测试的效果去郁敏myriocin,两种药物,阻止神经酰胺的合成,对果蝇的缺乏iPLA2-VIA基因,“犬吠说。“正如预期的那样,这两种药物导致的细胞减少大量的天然保湿因子。有趣的是,变异果蝇与药物治疗也提供更少的神经退化,减少爆炸敏感性,改善electoretinograms和溶酶体的变化与变异果蝇相比不是治疗药物。”
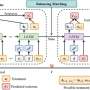
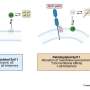
这些结果进行深入分析,研究人员调查的过程细胞使用重用和回收ceramide-derived脂质存在于细胞膜。细胞重用和回收这些细胞膜脂质保持平衡供应。重用这些细胞通过胞内贩卖retromer介导的脂质。Retromers可以识别这些脂质提取回收之前,把他们回到膜。脂质不重用以这种方式运输到溶酶体分为天然保湿因子,然后纳入膜的细胞。神经酰胺水平的增加变硬膜。这进一步扰乱了retromer的功能,从而导致更多的脂质穿梭的溶酶体分解产生更多的天然保湿因子。这将创建一个正反馈循环,导致神经酰胺积累并导致神经退化。
其调查结果显示线索表明神经酰胺平衡是苍蝇缺乏iPLA2-VIA基因的中断。这些变异果蝇Vps35和Vps26水平下降,蛋白质在retromers至关重要的功能。研究人员发现,通常iPLA2-VIA蛋白结合Vps35 Vps26和约束力的增强retromer函数。iPLA2-VIA蛋白质缺乏会导致更少的Vps35 Vps26 retromer函数的破坏原因,表明iPLA2-VIA蛋白稳定retromers及其功能,之前不知道。
“这些观察让我们预测,如果retromers是有缺陷的,溶酶体就有额外的工作,应该扩大,这就是我们所观察到的,“犬吠说。“我们测试的所有方法,改进retromer函数也导致了一个改进的缺陷我们观察果蝇缺乏iPLA2-VIA基因。有趣的是,vps35基因的突变也导致帕金森病。”
犬吠和他的同事确认这些结果在脊椎动物神经元生长在实验室。
此外,研究人员发现有高水平的α-突触核蛋白,帕金森病的一个特点在脊椎动物神经细胞,导致retromer功能障碍,溶酶体扩张和神经酰胺积累。有趣的是,这些缺陷引发的α-突触核蛋白过剩也减少了相同的治疗药物,提高了缺陷缺乏iPLA2-VIA基因在果蝇。
总之,这项工作提供了新的证据表明新和之前确认的部件之间的连接与帕金森病相关的难题并提出一种机制,可能导致的条件。
“我们表明,磷脂酶PLA2G6损失导致神经酰胺积累,缺陷retromer功能,进步溶酶体扩张和,最后,与共同的特征与渐进性神经退化观察帕金森病。和相同的药物,干扰神经酰胺的合成也改善了条件。我们还发现一个地方的α-突触核蛋白病难题,”林说。
“我们认为我们的工作很重要,因为它指向一个潜在的机制导致帕金森症和帕金森病,也许“犬吠说。“我们建议磷脂酶PLA2G6损失或减少Vps35原因中断retromer函数创建一个阴险的压力的细胞,可能是在这些条件的根源。如果retromer功能中断,神经元不能重用一些ceramide-derived脂质,和更多的人旅游到溶酶体,随着时间,更加努力地工作,因此开始扩大。另外,随着神经酰胺衍生脂质穿梭到溶酶体生产天然保湿因子,细胞建立天然保湿因子,重新分配的细胞膜和其他膜的细胞器,如线粒体,破坏细胞膜的功能。我们建议的途径逐渐变得越来越不安,因为膜硬化置入到神经酰胺,逐步创造了更大的压力以及线粒体功能障碍,最终将导致帕金森症和帕金森病从长远来看。”
更多信息:细胞代谢(2018)。DOI: 10.1016 / j.cmet.2018.05.019