一个可靠的、易于使用的小鼠模型为研究骨转移
在发表的一项研究自然通讯,一组研究人员由孝宏Kuchimaru和Shinae Kondoh东京理工学院(日本技术)提出了一种改进的小鼠模型,可以彻底改变骨转移的研究。他们的方法,包括通过所谓的尾动脉注射癌细胞在老鼠的尾巴,克服了许多传统的小鼠模型的局限性。新模型可以打开新的篇章为骨转移治疗策略的发展和癌症进展。
人们普遍知道metastasis-the传播癌症细胞从原发肿瘤的其他部分相对应的主要原因之一癌症人类的死亡率。骨转移通常发生在癌细胞扩散到骨从肿瘤始发,例如,前列腺癌、乳腺癌、肺癌和肾脏。
实验鼠标模型提供了重要的线索如何开发癌细胞增殖和如何治疗。在过去的20年,模型基于心脏内的(IC)注入被认为是诱导骨转移的“黄金标准”。这个模型是将肿瘤细胞直接注入老鼠心脏的左心室。它需要高度的技术专长,即使执行成功,肿瘤细胞的数量,可以注入任何时候是有限的。集成电路模型的另一个缺点是往往是更适合研究癌症细胞系具有相对较高的转移能力,排除“弱”的分析癌症细胞系。
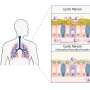
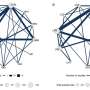
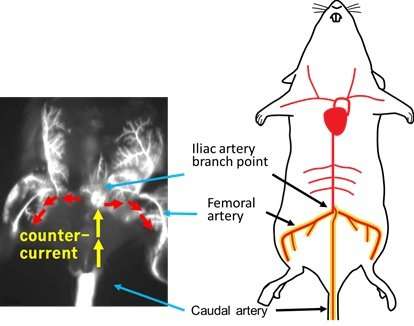
相比之下,新方法由Kondoh集团涉及注射癌细胞通过尾动脉(CA)的老鼠的尾巴——程序可以更容易地执行身体表面的动脉是可见的。(见图1和图2)。这种方法允许研究人员注入更多的肿瘤细胞而不造成急性死亡:在目前的研究中,一百万左右细胞被注入了没有任何急性死亡。此外,新方法提供了一种新的学习方式与低骨转移性癌症细胞系的潜力。
研究人员强调,CA模型主要是确保骨转移发展的后肢和更高的效率。
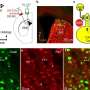
使用生物荧光成像(提单),团队能够发现骨转移后五到十二天CA注入的细胞系。
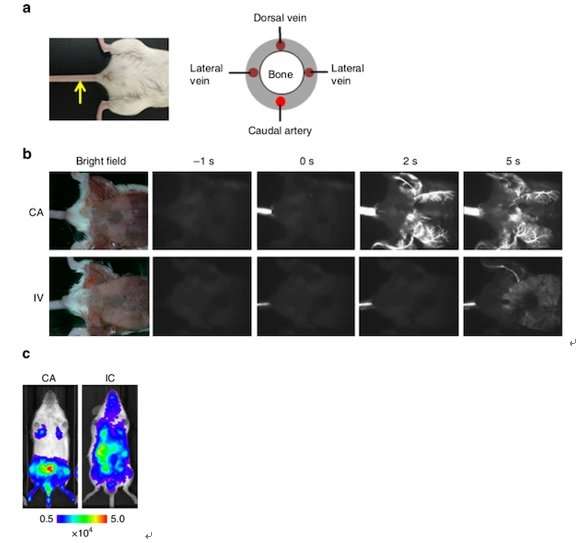
“总的来说,结果表明,CA注入提供了一个可靠的方法来开发骨转移通过增加输出效率的各种癌症细胞系小鼠后肢的骨髓,”他们写道。
此外,CA模型允许科学家们监测骨转移的进展在更长一段时间与集成电路模型相比,由于减少了致命的发病率在其他器官转移。这是一大进步在深入调查癌细胞休眠和复活。
研究人员得出结论,“我们的模型可能会打开一个新的途径了解药物预防骨转移过程和发展骨转移和复发。”
更多信息:孝宏Kuchimaru et al,可靠的骨转移小鼠模型通过尾动脉注射癌细胞,自然通讯(2018)。DOI: 10.1038 / s41467 - 018 - 05366 - 3