修复多发性硬化症损伤的新路线图
这项研究今天发表在杂志上自然提供了关于药物如何修复导致多发性硬化症患者残疾的受损脑细胞的新认识。由凯斯西储大学医学院的研究人员领导的这项研究表明,新的药物靶点和有效的早期候选药物可能会导致多发性硬化症和其他使人衰弱的神经系统疾病的再生药物。
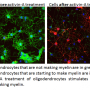
多个硬化神经萎缩症是一种慢性进行性疾病,影响着全球数百万人,其特征是神经细胞周围的保护鞘受损。如果没有这层叫做髓磷脂的绝缘层,大脑和脊髓中的神经细胞就很难传输电脉冲。结果,多发性硬化症患者逐渐丧失运动技能、视力和平衡能力。
这项新研究描述了药物如何补充被多发性硬化症破坏的髓磷脂。虽然已知大脑在多发性硬化症的早期阶段有一定的能力再生新的髓磷脂,但随着疾病的发展,这种先天的修复过程被淹没了。
包括凯斯西储大学在内的许多实验室已经确认候选药物凯斯西储大学医学院新疗法教授、遗传学和基因组科学助理教授德鲁·亚当斯博士说:“这些分子是如何影响脑细胞功能的还不清楚。”“我们震惊地发现,几乎所有这些之前确定的分子都具有抑制特定酶的能力,这些酶有助于制造胆固醇。这一见解将药物发现工作重新定位到这些新颖的可药物靶标上。”
这项研究建立在合著者Paul Tesar博士、Donald博士和Ruth Weber Goodman创新疗法教授以及凯斯西储大学医学院遗传学和基因组科学副教授之前的工作基础上。在2015年的工作报告中自然在美国,特萨发现了一种通常用于治疗脚气的药物咪康唑(miconazole),它能有效增强新髓磷脂。
在目前的研究中,Adams和Tesar领导的团队证明,咪康唑通过抑制脑干细胞产生胆固醇的一种酶来促进髓鞘的形成。随后的实验发现了20多种新药,它们通过抑制密切相关的胆固醇生成酶来促进髓磷脂的形成。令人惊讶的是,以前被世界各地的实验室鉴定为增强新髓磷脂的药物也抑制了这些酶。Tesar说:“几乎所有促进髓鞘修复的候选药物都抑制相同的酶靶标,这一想法代表了该领域的一个大胆的新范式,可能会重新引导正在进行的药物发现工作的进程。”
正常情况下,细胞通路是交叉的,复杂的图表。但胆固醇的生物合成是线性的,亚当斯说,他也是西奈山学者。“只有一条路进去,也只有一条路出去。所以当你阻断胆固醇途径中的酶时,代谢物就会堆积起来。”在亚当斯实验室,主要作者Zita Hubler和Dharmaraja Allimuthu博士可以检测到不同的胆固醇中间体,使他们能够确定哪些酶被哪种药物阻断。
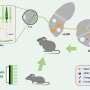
值得注意的是,几种药物加速了多发性硬化症小鼠模型的髓鞘修复。小鼠实验是与罗伯特H.米勒博士合作进行的,他是乔治华盛顿大学医学与健康科学学院的薇薇安吉尔杰出研究教授和解剖学和细胞生物学教授。
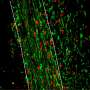
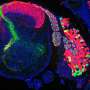
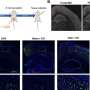
为了在实验室中测量人类髓磷脂的形成,该团队使用了一种新的三维神经细胞培养模型,该模型密切模仿人类脑组织。在这里,候选药物也通过阻断胆固醇途径酶促进人类髓磷脂的形成。在Tesar实验室开发的一项描述这一创新模型的研究今天也发表在自然方法.
Adams说:“这些研究共同提供了新的药物靶点、新的候选药物和新的胆固醇通路生物标志物,以推动药物的开发,以补充多发性硬化症和相关疾病患者失去的髓磷脂。”作者说,虽然基于这项工作的临床候选药物预计要到2019年才能进入临床试验,但对药物的新认识髓鞘修复为新型再生多发性硬化症治疗提供了一条有前途的新途径。