模拟肺部疾病的第一个小鼠模型可以加快发现更有效的治疗方法
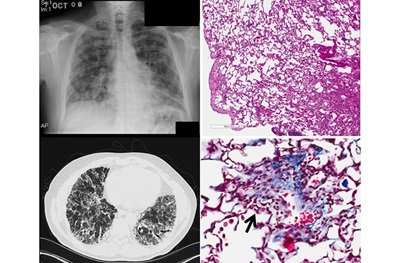
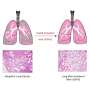
寻找特发性肺纤维化(IPF)有效疗法的最大障碍 - 一种威胁生命的疾病,肺部变得疤痕和呼吸越来越困难 - 无法完全模拟动物的疾病,限制了观察和观察和观察的能力了解疾病。现在,一支来自Penn Medicine的研究人员的团队开发了第一个具有IPF相关突变的小鼠模型,该模型诱发了疤痕和其他类似于患有这种情况的人类的损害。研究结果本周在临床调查杂志。
高级作家Michael F. Beers博士说:“迄今为止,没有人能够制作一个模型,这实际上反映了人类的情况。”宾夕法尼亚大学大学,宾夕法尼亚州肺部疾病中心的研究主任。“现在,我们有了一个模型,类似于患者中发现的病理,生理和分子体征,这将使我们能够以更临床相关的方式来制定新的途径和靶标,并测试药物。”
IPF经常在中期到更晚的阶段被诊断出在美国大约有50,000人,同时杀死了近40,000人。虽然无法治愈,但使用两名美国食品药物管理局(FDA)批准的药物来减缓疾病的进展,有些患者接受肺移植。自诊断之时起,中位生存率为两到三年。
Beers说,当前的IPF小鼠模型依靠化学疗法药物来诱导肺部的“炎症风暴”,该肺部大约在21天后引起病变。但这并不能反映人类发展疾病时实际发生的过程。
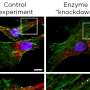
在新的鼠标模型,该团队改变了一个基因,用于制造一种称为表面活性剂蛋白-C(SFTPC)的蛋白质,这对于肺功能至关重要。SFTPC基因中的突变,在某些人类肺细胞中发现了称为肺泡上皮细胞(AEC)是归因于该疾病的一种有前途的铅。
该团队知道这些肺AEC在疾病发展中的重要性,将SFTPC突变诱导到正常小鼠的AEC中,以引起反应。在成年小鼠诱导突变体SFTPC表达的三天内,肺组织被炎症细胞浸润。随后是肺部微小气囊内炎症细胞异常积累。在30%至50%的动物中也观察到了快速死亡。与患者中观察到的相似,幸存的小鼠继续发展进行性纤维化和丧失肺功能。
使用新的动物模型,研究人员接下来将研究导致肺纤维化起始和持久性的途径。“现在问题变成了,为什么这些上皮细胞吸引两者炎性细胞和纤维化细胞?这些不同的细胞如何互相交谈?”啤酒说。
“我们也在大数据啤酒补充说:“通过在不同时间点上分析小鼠的遗传,蛋白质组学和炎症变化,从而接近。您不能在人类中这样做,因为我们一旦他们的疾病已经发展,我们就会看到这些患者。我们对一开始会发生什么知之甚少。该模型将有助于回答其中的一些问题,并希望导致更有效的治疗药物减慢疾病。”
进一步探索