研究人员发现了潜在的致盲性疾病的新基因疗法
去年见证了基因治疗领域的里程碑,FDA批准治疗癌症和遗传性致盲障碍。宾夕法尼亚大学(University of Pennsylvania)视觉科学家领导的团队的新发现正在被证明是成功的,他们过去曾将基因疗法带入临床试验,这次是治疗一种色素性视网膜炎,这种疾病在失明之前逐渐剥夺了人们的夜间视力和周边视力。
宾夕法尼亚大学兽医学院(Penn's School of Veterinary Medicine)和佩雷尔曼医学院(Perelman School of Medicine)的研究人员与佛罗里达大学(University of Florida)的科学家合作,开发了一种疗法,可以有效地消除视紫红素(一种感光分子)的异常复制,然后用该蛋白质的健康复制使其恢复。这种抑制和替代方法保存了受影响狗的视网膜感光细胞,这些细胞可能会发展成与受影响人类非常相似的疾病。
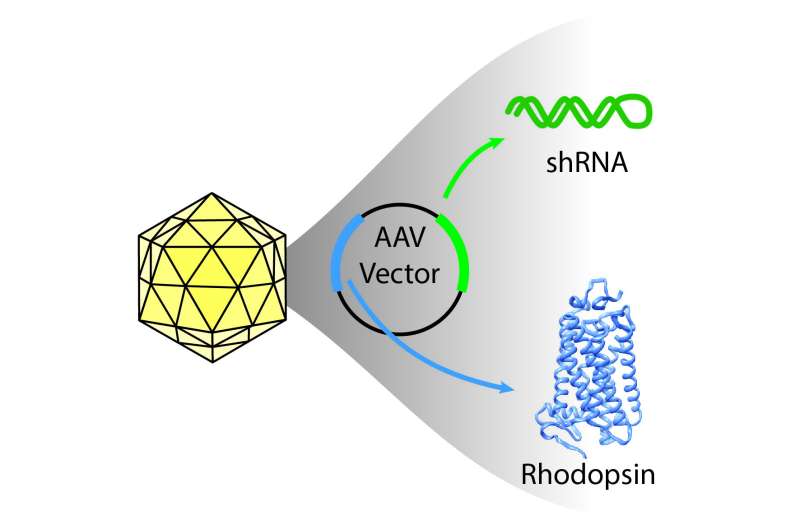
更重要的是,他们利用一个单一的病毒载体来共同传递达到敲除和替换所需的遗传物质。尽管已有超过150种不同的视紫质突变被鉴定为引起色素性视网膜炎的原因,但无论突变是什么,或者视杆细胞(在昏暗的光线下负责视觉的细胞)的死亡机制如何,这种方法都能起作用。这意味着,如果发现该疗法在人类中是安全有效的,那么患有视紫质常染色体显性视网膜色素变性的患者的很大一部分可能会受益。
“这是一种适合所有人的治疗方法,”威廉·a·贝尔特兰(William a . Beltran)说,他是眼科教授,也是宾夕法尼亚大学兽医学院实验性视网膜治疗部主任,也是这项研究的共同主要作者美国国家科学院院刊。“这种治疗针对的是人与狗的视紫红质基因的同源区域,与突变所在的位置是分开的。这给了我们巨大的希望,使其成为一种转化治疗。”
“几十年来,我们已经知道,这种特定的分子会导致一种特定形式的视网膜色素变性,但开发一种治疗方法并不简单,”宾夕法尼亚大学医学院(Penn Medicine)的眼科研究教授、论文的共同第一作者Artur V. Cideciyan说。“现在,基于对狗狗多年的研究,我们可以开始研究治疗这些突变,防止人类感光细胞恶化。”
这项工作是宾夕法尼亚大学视觉科学家长期合作的最新成果。除了Beltran和Cideciyan,这个团队还包括了宾夕法尼亚大学兽医学院(Penn Vet)的Beltran实验室研究助理Raghavi Sudharsan、医学遗传学和眼科教授Gustavo D. Aguirre,以及宾夕法尼亚大学医学院(Penn Medicine)的塞缪尔G. Jacobson,后者是眼科教授兼遗传性视网膜退化中心(Center for遗传性视网膜退化)主任。
色素性视网膜炎是指一组进行性遗传性视网膜疾病。30年前,研究人员发现了编码视紫质的基因突变,这是已知的导致这种疾病的第一个遗传原因。其他基因也有牵连,但红紫质突变仍然是主要原因,占常染色体显性视网膜色素变性的30%。
绝大多数的紫质突变以一种显性的方式在家族中传递,这意味着父母只需要传递一个突变副本,他们的孩子就会受到影响。
雅各布森说:“在我们的调查中,我们在20世纪90年代看到过患有这种遗传性色素性视网膜炎的人,现在我们看到他们的孙辈也受到了影响。”“这是一种多代疾病,而且是一种严重的疾病。”
导致色素性视网膜炎的几个视紫质突变导致了所谓的毒性功能获得,被认为会产生一种对感光细胞有害的蛋白质。因此,为了解决这些患者中出现的问题,研究人员确定最佳策略是消除突变蛋白。
Aguirre说:“在过去,我们已经开发了基因疗法来治疗突变导致功能丧失的其他情况,所以在这些情况下,我们只需要添加正常的基因副本,以便光感受器恢复正常的结构和功能。”当你患有像这种显性疾病时,基因产物会对细胞造成损害,你必须摆脱它。”
该团队早些时候的努力就是为了做到这一点:简单地敲除变异狗和正常狗的视紫质。这预防了疾病,但导致了关键细胞腔的杆状光感受器的丢失,也就是外部部分,它提升了视觉。Beltran和他的同事们确定,添加一个健康的副本将是实现健康视网膜细胞功能的最好和必要的策略。
在目前的工作中,研究人员采用了这种策略,它既依赖于体外分析,更重要的是,依赖于一个在红紫质基因中自然发生突变的犬类动物模型,该模型真实重现了由红紫质B类突变引起的人类视网膜色素变性的形式。虽然A类突变的视紫红质患者在生命早期失去了具有功能的杆状感光细胞,但B类突变的患者可能会保留他们的杆状细胞数十年,使其成为保留视力的基因治疗的候选对象。
因为突变的视紫质犬对环境光线非常敏感,所以用相当于正午亮度的短时间暴露来加速光感受器的退化。这种敏感性使研究人员能够控制视网膜的哪个部位以及什么时候最受影响,从而在几周内评估治疗成功与否,而不是在没有这种触发器的情况下需要数年时间来评估治疗成功与否。
在实验室中,该团队证实,他们可以通过使用一种叫做短发卡RNA (shRNA)的敲低试剂来破坏突变的视紫质基因,该试剂是由佛罗里达大学的Alfred Lewin和他的同事设计的,目标是基因突变部分之外的区域。添加一个健康的对这种shRNA有抗性的视紫红质基因的拷贝来补偿这种敲除。
在带有紫质突变的狗身上,他们使用了同样的策略,当shRNA和健康的紫质副本同时在同一个载体中传递时,而不是使用两个不同的载体时,他们获得了最好的成功。研究小组恢复了大约30%正常水平的视紫质,足以防止视网膜杆状细胞的恶化。
“我们所展示的是,如果你只进行敲除,你就可以保存杆状细胞的外核层,也就是细胞体所在的地方,”贝尔特兰说。“但如果没有另一个关键层,即外部部分,在那里视紫质起着捕捉光线和启动视觉的重要作用,视杆细胞就会变得无用。”然而,如果你把敲除试剂和替代试剂结合起来,那么巨大的区别就在于你现在已经完美地形成了对齐的外节段和有功能的感光细胞。”
宾夕法尼亚大学研究人员能够确认有利影响两个视杆细胞的结构和功能(以及锥,负责色觉)通过使用专门的成像技术,可以使用在人类患者随着electroretinography,它提供了一个衡量的视杆细胞和视锥函数。
到目前为止,跟踪治疗效果超过八个月后,基因治疗的效果似乎是稳定和持久的。该研究小组目前正致力于将研究结果转入临床试验。
Cideciyan说:“目前的工作对由于B类视紫红质突变而导致的常染色体显性视网膜色素变性患者的治疗具有很强的意义。”
进一步探索








用户评论