基因变异揭示了慢性肾脏疾病治疗的新靶点
肾脏的功能是其他器官的两倍甚至三倍——提取废物、平衡体液、形成尿液、调节血压和分泌激素。考虑到这种复杂性,一旦出现问题,就会造成严重破坏,导致一系列被称为慢性肾病(CKD)的症状,包括毒素积聚、疲劳和高血压。
通过研究基因变异如何驱动基因表达基因根据宾夕法尼亚大学佩雷尔曼医学院肾电解质、高血压和遗传学教授Katalin Susztak博士领导的一项研究,在肾脏的过滤细胞中,研究人员发现了解释CKD发展的新途径,并可以为其治疗提供信息。Susztak和他的团队在自然医学这个星期。
今年早些时候,Susztak的实验室生成了肾脏图谱,其中包括肾脏中所有细胞类型的新颖分子定义。他们得出的结论是,每种不同类型的CKD都有独特的、非冗余的功能,特定的功能障碍与CKD患者的特定症状相关。从这一点开始,团队开始了解如何做到这一点肾脏疾病在单细胞水平上发展。
Susztak说:“这项研究首次研究了特定的细胞类型,以及它们的遗传变异如何导致疾病的发展。”
慢性肾脏病是一种肾脏无法清除废物的疾病,全球有7亿人患有这种疾病。根据美国国家糖尿病、消化和肾脏疾病研究所的数据,美国CKD的总体患病率约占总人口的14%。
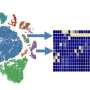
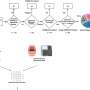
该团队创建了一个数据库来展示如何做到这一点遗传变异影响信使RNA的表达肾细胞.通过将CKD相关全基因组关联分析(GWAS)的信息与更具体的方法相结合,研究人员确定了与CKD相关的基因和细胞。GWAS收集了不同个体中特定基因的DNA构建单元顺序的一组变异,以确定任何变异是否与某种疾病或特征相关。
“在过去,许多GWAS工作已经确定了CKD的序列变异,但这些变异的生物学基础知之甚少,”Susztak说。“我们需要利用GWAS数据库中的所有信息做更多的工作,以确定导致CKD的基因、细胞和分子途径。”
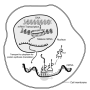
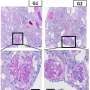
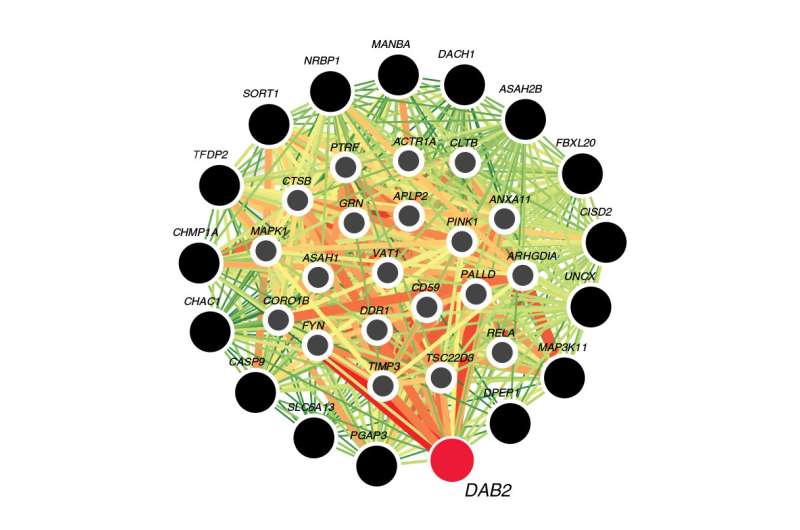
研究小组发现,通过单细胞RNA测序分析,被认为导致CKD-27的候选基因在肾近端小管中表达更丰富。肾小管是肾脏精细过滤器的一部分,尿液中的营养物质被重新吸收。从这27个基因列表中,他们最初专注于一个基因,TGF-β通路中的适配器蛋白DAB2,并发现它与许多其他基因有关肾脏函数。
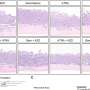
使用两种类型CKD小鼠模型的进一步实验证实,减少小管中DAB2的表达可以保护小鼠免受CKD的影响。通过降低DAB2基因的表达,细胞因子TGF-β通路在错误的伤口愈合反应中不会诱导纤维化。
将这一知识推向临床还需要几个步骤,Susztak说:“我们刚刚开始寻找哪些分子误入歧途导致了疾病,以便开发药物来抵消对健康组织造成损害的过度活跃的分子。”