沃尔特里德陆军研究所开始第一阶段马尔堡病毒疫苗的临床试验
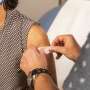
沃尔特里德陆军研究所(WRAIR)本周第一次疫苗接种1期临床试验评估马尔堡候选疫苗的安全性和免疫原性在健康成人志愿者。
WRAIR研究评估VRC-MARADC087-00-VP疫苗开发的疫苗研究中心(VRC)国家过敏症和传染病研究所(NIAID),国立卫生研究院(NIH)。黑猩猩重组腺病毒类型3-vectored马尔堡病毒候选疫苗正在测试旨在刺激快速而持久的免疫力。这种疫苗接种策略被认为是最佳的保护一线卫生工作者和一般人口的地区疫情发生。
“鉴于最近致命爆发马尔堡病毒在乌干达,急需开发一种安全有效的疫苗,它有可能保护我们的士兵和公众从这个严重的威胁,”梅林达•哈默尔中校说WRAIR临床试验中心的银泉,试验正在进行。
四十健康成人志愿者将登记和分配分为两个组来评估不同剂量的疫苗。志愿者们将密切关注在大约一年后疫苗安全性和免疫系统的反应。
的是在同一个家庭埃博拉和马尔堡病毒引起人类严重的出血热。病死率在马尔堡出血热暴发范围从24%到88%。在2017年最近的爆发发生在乌干达。
WRAIR进行第一次埃博拉病毒疫苗临床试验于2009年在非洲,测试早期候选疫苗也在NIAID VRC开发的。在2014年的西非埃博拉病毒疫情,WRAIR构思,然后发起一个VSV-EBOV的I期临床试验候选疫苗在一段时间内的11周CTC。WRAIR六埃博拉病毒疫苗进行了研究。
“这first-in-human审判的美国国立卫生研究院疫苗是一个重要的一部分,由美国政府机构间努力预测和应对新兴传染病威胁美国,无论在军事还是民用方面国内外,”博士补充说Kayvon Modjarrad, WRAIR新兴传染病部门的主任。