酶的免疫细胞在宿主防御肺结核中扮演不可或缺的角色

使用新鲜切除肺组织来自21个病人和两个不同的小鼠模型,结核病在伯明翰的阿拉巴马大学的研究人员和非洲卫生研究所或AHRI,分离出一种蛋白质中扮演着重要的角色在宿主防御这致命的疾病。
这项研究由安德利“Adrie”Steyn说,博士,一位阿拉巴马大学的微生物学教授在阿拉巴马大学和维护实验室AHRI,在德班,南非。由于结核病率很高,或结核病,在南非,感染人类肺组织很容易就可以从附近的医院,病人接受手术恢复作为最后的希望。
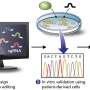
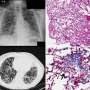
直接研究新鲜肺tissue-including microanatomic利基市场的健康和严重患病的地方那么可以揭示免疫反应和细胞活动的差异在这些不同的区域。Steyn说,他的研究小组说,这种独特的方法将帮助识别潜在的宿主因素,可以治疗针对限制广泛的组织损伤与慢性肺结核疾病有关。这种危险的肺组织,包括肺部感染耐多药和广泛耐药结核病的细菌,仔细地处理在一个先进的生物安全实验室AHRI因为只有一到三个结核细菌气溶胶飞沫可引起感染。结核感染结核分枝杆菌,结核分枝杆菌或,杀死每年大约有130万人。
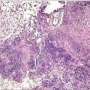
该和他的同事们能够区分不同类型的细胞发现在不同的领域人类刚切除肺部结核和描述这些细胞血红素oxygenase-1生产蛋白质。血红素oxygenase-1 HO-1,是一种酶,这种酶能保护细胞免遭有害活性氧和氮中间体;HO-1也是可以控制炎症反应。
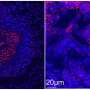
研究人员发现,人类结核病HO-1肺表达主要由骨髓免疫细胞,包括中性粒细胞和巨噬细胞,HO-1水平在这些细胞直接正比于防止结核病病理生理学。
具体来说,有一个更大比例的HO-1-producing中性粒细胞和巨噬细胞在肺部的感染区域病变区域,和这些细胞在感染地区HO-1比细胞病变区域。因此,缺乏HO-1保护病变区域允许破坏性的骨髓细胞活性氧和氮物种。使这些发现临床相关的是HO-1是必不可少的在人类而不是老鼠,它指向的重要性研究人类结核病肺组织为结核病补充动物模型。
“尽我所知,这个新人类结核病切除肺组织的广泛分析是第一的,因为这些肺稀缺,”该组织表示。
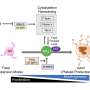
这一发现对人类是由两个HO-1缺乏小鼠模型显示HO-1是必要的控制骨髓细胞浸润和炎症预防结核病恶化。一个小鼠模型是一个全球HO-1基因的敲除;另一个模型是一个HO-1淘汰赛髓细胞只有。在这两种模型,基因敲除小鼠结核分枝杆菌更容易感染后基因敲除小鼠死的越早,更高的结核分枝杆菌的肺脏和脾脏。基因敲除小鼠也有渗透免疫细胞和细胞因子水平的增加,细胞信号蛋白调节或刺激免疫反应。
总的来说,人类肺部和小鼠模型的结果显示,HO-1表达,特别是在骨髓细胞,似乎是结核分枝杆菌宿主防御疾病进展的关键。Steyn说,人类结核病患者的研究表明,寻找方法移植HO-1活动期间可能会限制免疫病理疾病活动性结核病。
这个研究发表在《华尔街日报》11月13日细胞的报道,也出现在杂志的封面。
两个实验室,一个世界
Steyn说教授和初级教员UAB UAB的微生物学和维护一个研究实验室。他也是一个全职研究员AHRI和生活在德班,南非。他访问UAB每年至少6次。
Steyn说负责创建一个程序,学生从阿拉巴马大学的研究生院、医学院获得一个独特的机会去和AHRI行为研究作为研究的一部分,培训实习。“一旦你去非洲的偏远地区,看到疾病的破坏,”该组织说,“它只是改变你。它使不同。”
在AHRI给学生,特别是在医学培训项目,一个极好的机会工作先进的研究设施位于一个最高的国家之一的国家在全球疾病负担。七名阿拉巴马博士和医学博士/博士。学生所做的研究在德班Steyn说的实验室作为年度夏季UAB-AHRI国际研究项目的一部分。
该组织的细胞的报道工作之前研究还使用人类结核病的肺部组织。研究发表在去年5月在免疫学前沿Steyn说和他的同事,检查铁病变肺部结核的分布。铁是结核分枝杆菌的生长和毒力的一个重要因素,但很少有人知道如何在感染主机控制铁的可用性。
该和她的同事发现铁蛋白H铁储存蛋白质的重要作用在结核病的控制,这是与HO-1直接相关。研究人员发现,小鼠模型,有铁蛋白重链基因的敲除髓细胞更容易感染结核病,如图所示在器官结核分枝杆菌的数量增加,更多的结核分枝杆菌的传播以外的肺部和减少生存。值得注意的是,铁的水平被发现在人类结核病的肺。
进一步探索