可以治疗手术粘连,在小鼠中预防
斯坦福大学医学院的研究人员确定了一种常见的,有时威胁生命的后手术后并发症的蜂窝罪魁祸首,以及可能的治疗方法。
当异常的纤维连接在腹部手术,将我们通常的滑动器官绑在一起,或将它们锚定在腹壁上。症状可能包括慢性疼痛,女性不育症,肠梗阻以及偶尔死亡。根据美国国立卫生研究院的数据,在美国治疗后手术后粘附的年成本超过10亿美元。
“这是一个非常常见的外科手术并发症,但没有得到充分研究,”斯坦福大学的前医学生乔纳森·泰(Jonathan Tsai)博士说,现在是波士顿布里格姆(Brigham)和妇女医院的住院医师。“到目前为止,甚至还不知道哪种细胞类型涉及来源的粘连。现在,我们已经提出了一种在形成粘连并鉴定涉及的分子途径之前分离出受伤组织的方法。”
研究人员开发并研究了一个鼠标模型粘附编队以识别负责初始步骤的单元格。他们还表明,基于抗体的疗法可能会分解已经形成的疗法。希望是类似的技术可以帮助治疗人类的术后粘附。
Tsai是该作品的主要作者,该作者将于11月28日在科学翻译医学。尤瓦尔·林克维奇(Yuval Rinkevich)博士是前斯坦福大学博士后学者和病理学和发育生物学教授欧文·魏斯曼(Irving Weissman),分享了该研究的高级作者。魏斯曼(Weissman)是斯坦福大学干细胞生物学和再生医学研究所以及斯坦福大学路德维希癌症中心的主任。
研究人员发现,两种抗体的组合 - 一种针对的细胞负责粘附的形成,另一个沉默的“不要吃我”的信号表明癌细胞用来逃避免疫系统 - 可以显着降低动物中已建立粘连的严重程度。
魏斯曼说:“尽管我们使用小鼠模型研究了粘附形成,但我们发现患者的粘附特征相似,这使我们认为这种方法可以转化为诊所。”
常见的并发症
通常,我们的腹部器官的表面和腹腔的衬里被称为间皮的湿滑膜覆盖。当我们弯曲,扭曲或奔跑时,间皮使我们的器官彼此平稳滑行。当间皮受到干扰时,相邻表面之间形成了纤维连接,从单线到巨大的,固定的网络的严重程度。NIH估计,大约93%的腹部手术会导致粘连,并且大约20%的手术患者将被重新住院以治疗与粘附相关的并发症。
尽管并发症很普遍,但并不是很容易理解。研究人员已经确定了该过程后期步骤中涉及的一些细胞类型,但是尚不清楚哪种细胞类型是对初始步骤的原因。它似乎是在受到血液流动受到限制的区域中产生的,例如在由手术缝合线引起的组织小捏中。结果,较少的氧气被输送到该区域的细胞 - 一种称为缺氧的疾病。
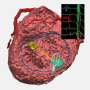
TSAI使用该条件的小鼠模型来追踪间皮中基因表达的粘附形成和所得的基因表达模式。
Tsai说:“我们发现受伤后的间皮细胞产生粘附。”“通过追踪基因表达的模式,我们能够为这些纤维化组织提出一个细胞的'家谱',并确定所涉及的生物途径。”
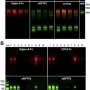
Tsai及其同事发现,在小鼠中,间皮细胞通过制造称为HIF1Alpha的蛋白质来应对缺氧。反过来,这促进了其他蛋白质的表达,这对于形成粘连所必需的。当研究人员用抑制HIF1Alpha活性的小分子治疗动物时,所产生的粘连明显不那么严重。
巨噬细胞的可能作用
他们还发现,用与间皮素结合的抗体(一种特有受伤的间皮的蛋白质)的抗体可显着降低已经形成的粘附的严重程度。将抗中皮蛋白抗体与抗CD47抗体结合起来,具有更大的作用,这表明将称为巨噬细胞的流动免疫细胞吞噬了病态或垂死的细胞,也可能在去除异常的纤维组织中发挥作用。
魏斯曼说:“当刺激间皮时,它开始表达间皮素,通常在发育中很早就表达。”“这引发了细胞的增殖,并引发了一种炎症性级联反应,该级联反应带来了免疫细胞和蛋白质,这些级联细胞和蛋白质与纤维组织相互弥补。但是,这些细胞在其表面上也具有CD47,我们发现抗CD47可以与抗CD47协同作用。- 在形成这些粘附后,可以去除这些粘附。”
最后,研究人员研究了已从患者中去除的粘附样品。他们发现,人体组织表达了许多相同的基因,并使用了与小鼠中研究人员相似的生物学途径。Tsai及其同事希望类似的基于抗体的疗法可以帮助预防或治疗人们的粘连形成。
进一步探索