新的小鼠模型可能加速有前途的肌肉萎缩症疗法的鉴定

马萨诸塞州总医院(MGH)的一个研究小组创建了一种常见形式的肌肉萎缩症的新小鼠模型,该模型具有快速区分有前景的治疗药物和不太可能成功的药物的潜力。在他们发表的报告中自然通讯他们还描述了测试一种新的反义寡核苷酸药物——一种合成的核酸链,它通过与蛋白质的mRNA分子结合来阻止蛋白质的转录——这可能更有效地阻止异常蛋白质的产生。
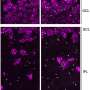
“这种新型荧光模型可以监测治疗性疾病药物该报告的资深作者、麻省总医院神经内科的瑟曼·惠勒博士说。“通过将已建立的1型肌强直性营养不良小鼠模型与表达红色或绿色荧光蛋白在肌肉中,根据目标RNA序列的剪接,我们开发了一个模型,其中肌肉在治疗前大部分是绿色的,在治疗成功后大部分是红色的。”
肌强直性营养不良是成人肌营养不良最常见的一种形式,有两种亚型。1型(DM1)影响RNA剪接,即从RNA分子中去除非编码片段并精确决定产生哪种蛋白质的过程。dm1相关突变影响编码骨骼肌中几种重要蛋白质的rna的剪接,以及参与胰岛素代谢和心脏功能的蛋白质。用现有的动物模型来确定潜在的DM1疗法是否可以纠正这种异常剪接,需要对肌肉组织进行分子分析,这既昂贵又耗时,而且需要大量的动物来测试每种新药。
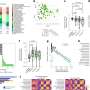
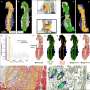
惠勒的团队将现有的用于细胞研究的基于荧光蛋白的系统改造为蛋白质只在细胞中表达的系统骨骼肌组织。在这个“双转基因”小鼠模型中,受DM1的异常RNA剪接影响的肌肉纤维发出绿色荧光,而剪接正确的肌肉纤维发出红色荧光。红色和绿色信号之间的比率表明是否潜在的治疗是纠正异常剪接。
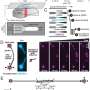
研究人员首先使用现有的反义寡核苷酸(ASO)对他们的模型进行了测试,ASO针对DM1中rna介导的疾病过程。他们惊讶地观察到,在将ASO注射到动物肌肉中三天后,红绿比就开始增加,而且这种增加持续了几周。注射后49天的肌肉组织分析证实了异常RNA剪接的修正。皮下注射另一种ASO可以纠正原始DM1模型中的RNA剪接缺陷,早在四次注射的第一次注射后14天,就产生了治疗效果,如红/绿比增加所示,在第25天的第8次注射时,效果变得更加明显。
因为之前测试ASOs作为潜在DM1疗法的研究受到了缺乏足够药物浓度的限制肌肉基于mgh的团队测试了一种称为配体共轭反义(LICA)的技术,该技术可以增强皮下注射ASO到全身肌肉的输送。他们的LICA ASO -第一个被测试为潜在的DM1治疗-表现出的治疗活性是相同ASO的未偶联版本的两倍,表明LICA药物的效力提高了两倍。
“我们的研究结果支持LICA技术在DM1治疗方面的进一步发展。除了新的ASOs,其他治疗策略,如小分子候选药物,siRNAs和蛋白质基于疗法也可以用它来测试模型.从长远来看,随着基因编辑治疗方法的普及,这将是测试基因编辑治疗方法的理想选择,”哈佛医学院神经病学助理教授惠勒说。“更快地识别有前景的治疗方法和早期排斥失败的候选方法,将有助于更快地为患者提供有效的治疗方法,并降低开发成本。”
更多信息:胡宁燕等,非侵入性监测替代剪接结果以确定肌强直性营养不良1型的候选疗法,自然通讯(2018)。DOI: 10.1038 / s41467 - 018 - 07517 - y