研究人员克服了CRISPR基因编辑肌肉萎缩症的障碍

被称为CRISPR的基因编辑技术是治疗遗传性疾病的革命性方法。然而,该工具尚未被用于有效治疗长期慢性疾病。密苏里大学医学院段东升博士领导的研究小组发现并克服了CRISPR基因编辑中的一个障碍,这可能为使用该技术进行持续治疗奠定基础。
CRISPR基因编辑的灵感来自人体抵御病毒的自然防御能力。这项技术使研究人员能够通过切除和替换基因组中的突变来改变DNA序列,这有可能治疗各种遗传疾病和病症。Duan和他在MU、美国国立卫生研究院国家转化科学推进中心和杜克大学的合作者正在研究如何利用CRISPR来治疗杜氏肌营养不良症(DMD)。
患有DMD的儿童有一种基因突变,这种突变会中断一种被称为营养不良蛋白的蛋白质的产生。没有抗肌萎缩蛋白,肌肉细胞变得越来越弱,最终死亡。许多儿童失去了行走的能力,失去了呼吸和呼吸所必需的肌肉心脏功能最终停止工作。
段教授说:“CRISPR本质上是切除突变,并将基因重新缝合在一起。bob88体育平台登录在慕尼黑大学医学院分子微生物学和免疫学系。“为了做到这一点,CRISPR中的‘分子剪刀’,即Cas9,必须知道从哪里剪。切割的位置是由一种叫做gRNA的分子标记的。我们惊奇地发现,通过增加标记的数量,我们可以将治疗的有效性从3个月延长到18个月小鼠模型."

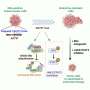
段的实验室使用CRISPR静脉内治疗了6周大的DMD小鼠,并在18个月时寻找改善。他们最初采用了一种被许多研究人员广泛使用的策略。在这种方法中,给予相似数量的Cas9和gRNA。虽然直接注射到肌肉中效果很好,但当团队试图在身体所有肌肉中实现长期矫正时,这种策略的效果很差。他们发现骨骼肌中没有肌营养不良蛋白的恢复,心脏中也有低水平的肌营养不良蛋白的恢复——治疗未能阻止疾病的进展。
在检查结果时,研究小组发现了不成比例的gRNA标记缺失,这意味着没有足够的gRNA来告诉Cas9在哪里切割。研究小组增加了gRNA标记的数量,并重复了这个实验。这一新策略显著增加了心脏和心脏肌萎缩蛋白的恢复骨骼肌并且在18个月时减少了肌肉疤痕。此外,肌肉功能和心脏功能也得到改善。
段说:“我们的研究结果表明,gRNA缺失是长期系统性CRISPR治疗的独特障碍。”“我们相信这一障碍可以通过增加和优化gRNA剂量来克服。虽然这为DMD疗法的改进带来了令人兴奋的可能性,但我们相信这一原理也可以应用于其他一系列疾病和病症的其他CRISPR疗法。”
在探索其他模型之前,研究人员将继续在小鼠模型中测试和完善这种方法。随着更多的研究,他们希望这一见解可能有助于为使用CRISPR基因编辑改进治疗奠定基础。
这项名为“AAV CRISPR编辑挽救营养不良小鼠18个月的心脏和肌肉功能”的研究最近在网上发表江森自控的洞察力.