Lypla1基因以性别特异性的方式影响肥胖

对肥胖、胰岛素抵抗和其他心脏代谢特征的易感性也可能取决于一个人的性别。加利福尼亚大学(UCLA)、Helmholtz Zentrum München (DZD的合作伙伴)和Ludwig-Maximilians-Universität München的一个国际研究团队研究了性别差异和性别特异性相互作用与心脏代谢表型的遗传背景。除此之外,研究人员还发现了Lypla1基因的一个性别特异性肥胖位点,该基因与人类肥胖有关。这项研究的结果已发表在细胞代谢.
男性和女性对肥胖、胰岛素抵抗和其他心脏代谢特征的敏感性可能不同。女性通常具有更有利的代谢特征。这在老鼠和人类身上都有描述。但性别是如何与基因相互作用的呢?自然遗传变异起什么作用?这是如何影响心脏代谢特征的发展的呢?为了回答这些问题,一个国际研究团队使用了一种动物模型(杂交小鼠多样性小组)在50个心脏代谢性状中寻找性别特异性差异。性别对心脏代谢特征的影响是根据与特定疾病表型的性别特异性相关性、它们的遗传结构和脂肪和肝脏中的潜在表达网络进行研究的。研究发现,性别(取决于遗传背景)在基因表达和心脏代谢性状的发展中起着重要作用。研究小组发现了Lyplal1基因的一个性别特异性肥胖位点。
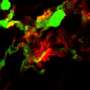
“此外,我们能够证明,白色脂肪组织的‘变白’有性别特异性的调节,线粒体功能有性别特异性的相互作用,”UCLA教授Aldons J. Lusis说,他是该研究的最后一位作者和负责人。棕色脂肪组织可以通过脂肪酸的氧化产生热量。这发生在线粒体中,线粒体也是组织呈现褐色的原因。如果“好的”棕色脂肪被激活,新陈代谢就会被刺激,“坏的”白色脂肪沉积就会减少。白色脂肪组织中出现棕色或米色脂肪细胞被称为“褐变”或“变黄”,这是一种与能量消耗增加有关的现象,至少在人体中是这样的小鼠模型可以预防肥胖。
目前的研究表明,女性线粒体活性更高,产生的线粒体也更多棕色脂肪组织.这可以减少脂肪量和胰岛素抵抗。在男性中,基因和性别之间的相互作用往往会导致低线粒体活性和低米色。体重和胰岛素抵抗增加。
“在参考文献中,已经有迹象表明,男女之间的脂肪生物学也存在重大差异。这项研究为代谢的性别差异的深度和广度提供了见解。我们相信,我们的研究结果提供了令人信服的证据,说明为什么男性和女性在生物研究应该作为一个整体来对待不同的有机体,而不是试图一次一个分子地调和这些差异,”DZD研究员、亥姆霍兹糖尿病中心糖尿病与再生研究所的医学博士苏珊娜·霍夫曼教授说。她的团队与Helmholtz中心München核心设施病理与组织分析的Axel Walch教授一起检查了脂肪组织并分析了勃朗宁的性别差异白色脂肪组织.
在理解这些性别差异背后的生物学方面仍有许多空白。因此,作为一个长期目标,研究人员希望开发一个生物网络模型,在系统层面上描述男性和女性之间的差异(“性组”)。这样的模型将需要识别作用于网络的主要和下游性别偏见因素,并理解性别偏见网络交互是如何产生的性别差异在突现表型中。
进一步探索