研究了激进的乳腺癌靶向治疗选择
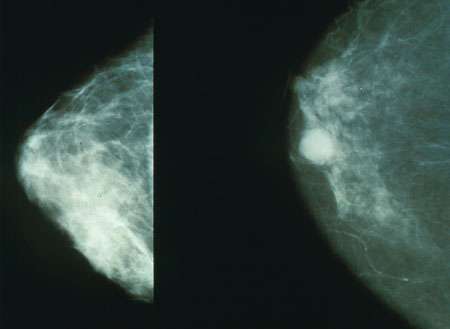
新发现马里兰大学费舍尔提出的生物工程学系(BIOE)和其他四个学术机构的研究人员大纲靶向治疗策略治疗三阴乳腺癌(TNBC) -一个潜在的第一个特别积极形式的乳腺癌。演示了在组的论文发表在今天自然纳米技术拟议的战略集中在基于纳米技术的精确定位的基因称为POLR2A。
大约10到20%的乳腺癌被认为是三阴性,这意味着,与大多数乳腺癌,这种不受荷尔蒙雌激素和孕激素,也由HER2蛋白质。
而对于大多数其他形式的治疗乳腺癌工作目标这三个途径之一,TNBC不应对现代荷尔蒙疗法或药物目标HER2蛋白受体。因此,大多数TNBC患者仅限于化疗作为他们唯一的全身治疗选项。
“由于缺乏靶向治疗的选择,TNBC患者往往面临贫穷的预后比其他类型的乳腺癌患者癌症BIOE小明教授说:“他(肖恩),论文的通讯作者。“虽然我们看到了引人注目的进步在乳腺癌治疗近几十年来,TNBC患者通常治疗与常规化疗常与副作用,药物耐药性,甚至癌症复发或复发。因此,迫切需要开发靶向治疗TNBC。”
所有癌症的产生是由于细胞内的基因发生了改变,或一组细胞。在的情况下三阴性乳腺癌,被称为TP53基因是最经常删除或突变。
但是,TP53是至关重要的。它提供了指令的p53蛋白,有助于防止肿瘤的发展通过阻止细胞突变或受损DNA生长和分裂失控。尽管许多研究人员认为技术恢复p53活动,没有这样的疗法已被翻译成诊所,由于p53信号的复杂性。
认识到这一点,他和他的研究团队已经努力关注POLR2A-an邻近基因TP53的必要手段。集团选择了这条路,因为基因组的改变往往是大型区域活动。大多数癌症导致的损失也一个特定的肿瘤抑制基因导致的部分损失如POLR2A附近的基因,基因是任何细胞生存所必需的。
尽管癌症细胞可以存活POLR2A的部分损失,他们变得弱,容易受到POLR2A抑制。知道了这一点,他和他的研究小组推测,靶向抑制POLR2A可能杀死TNBC细胞,同时保留正常细胞。
探索这个选项,研究小组与小干扰RNA核糖核酸干扰(RNAi)(核)生物过程RNA分子的抑制基因表达或翻译。这个过程可以用于几乎任何精确的目标基因包括那些可能导致肿瘤的生长。
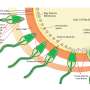
挑战,然而,核是极其不稳定的在核内体和溶酶体,血液和细胞的消化系统。为了克服这些障碍,研究小组设计的“nano-bomb”粒子,他们可以利用保护血液循环和携带POLR2A siRNA siRNA到靶向肿瘤细胞“吃”。The particles then generate CO2 gas to break open endosomes and lysosomes to ensure timely release of siRNA to inhibit POLR2A.
集团相信,他们的发现给人以希望,一天,一个基于纳米技术的精确定位策略可以用来打击TNBC和许多其他类型的癌症。
进一步探索