研究人员报告了乳腺癌细胞的一种新的可靶向脆弱性
赫尔辛基大学和卡罗林斯卡学院的研究人员发现了乳腺癌细胞信号传导的新的分子机制,这种机制有助于癌细胞的攻击行为。
癌症不受控制的生长源于细胞分裂和程序化调控的不平衡细胞死亡.为了刺激生长,癌症细胞可诱导多种信号受体;包括FGFR4受体酪氨酸激酶,其癌症促进信号通路仍不完全清楚。
在乳房癌症中,FGFR4在亚群中特别过表达,其中细胞增殖由另一种相关的信号受体HER2驱动。针对HER2的靶向治疗被用于有效治疗HER2阳性乳腺癌患者。因为在这些肿瘤中,FGFR4的过度表达与患者的生存率低相关,因此联合靶向FGFR4的药物可以阻止肿瘤的扩散,并提高那些尽管靶向HER2但肿瘤仍在积极扩散的患者的治疗效果。
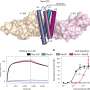
基于这一思路,Kaisa Lehti副教授领导的新研究通过筛选数千个可以被FGFR4介导磷酸化修饰的候选蛋白,首次全面阐明了FGFR4的功能。
Lehti说:“出乎意料的是,我们发现FGFR4有效地磷酸化了Hippo肿瘤抑制途径的几种基本蛋白质。”顾名思义,Hippo通路抑制不受控制的生长,Hippo通路信号通路的紊乱有助于肿瘤的生长。
对乳腺癌细胞的生化研究表明,FGFR4通过磷酸化MST1/2 Hippo激酶,不仅可以调节生长,还可以阻止程序化细胞的诱导死亡.在这些由HER2和FGFR4信号通路驱动的癌症中细胞被迫积极抑制程序性细胞死亡途径通过这里确定的机制生存和生长。
尽管这种复杂的癌细胞信号机制看起来很奇特,几乎不可战胜,但它们也为药物靶向提供了很大的机会。FGFR4受体具有独特的结构特征,可以与药物特异靶向,该类型的几种化合物已经用于基础研究和临床试验。在这项研究中,研究人员利用了一项全面的肿瘤药物测试,该测试表明,FGFR4靶向药物与HER2靶向治疗或细胞固有死亡程序调节剂相结合的治疗有效地降低了乳腺癌细胞的活力。
“这清楚地揭示了癌细胞信号传导的共同靶向脆弱性,这些有希望的结果为未来的研究提供了证据,以研究FGFR4靶向对抗HER2阳性乳腺癌或其他乳腺癌的潜力癌症FGFR4过表达的类型,”Lehti说。
研究结果发表在细胞死亡与分化.