关闭致命儿童脑癌在其最早的时刻
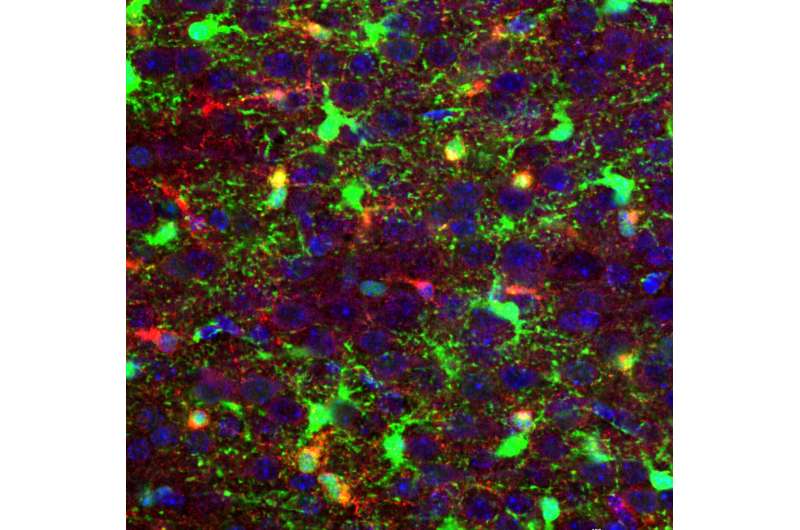
发展中新生儿小鼠脑组织细胞基因分析和实验室模型脑癌允许科学家发现分子高度侵略性的司机,致命的,和难治性脑癌,胶质母细胞瘤。
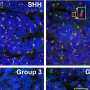
研究结果发表在细胞干细胞描述的单细胞分析确定了分组人口细胞至关重要胶质母细胞瘤形成研究少突细胞的早期原始的祖细胞大脑细胞,pri-OPC祖细胞,根据问:理查德·卢博士,首席研究员和科学的大脑肿瘤中心主任辛辛那提儿童医院医疗中心。
原始的数据表明,重组少突细胞祖细胞在神经胶质瘤干细胞样状态起着重要的作用起始和进展。研究者的主要分子目标在这项研究中,一种叫做Zfp36l1的蛋白质,生物程序启动镜像的健康小鼠早期大脑发育,而是帮助燃料的大脑肿瘤的生长。发现提供了一个机会来发现新的治疗方法可以停止在其初始形成的早期阶段或复发胶质母细胞瘤,陆说。
研究人员发现失调Zfp36l1-a蛋白结合在一起的不同RNAs-causes神经系祖细胞增长如此之快,他们承担的属性快速增长的干细胞样细胞癌变。这是尤其是欠发达的原始少突细胞祖细胞。这一发现给科学家一个主意。
“当我们使用小RNA-interfering分子抑制Zpf36l1基因的表达在老鼠和人类神经胶质瘤肿瘤细胞,它大大降低了神经胶质瘤细胞生长和传播的速度,”陆说。“基因敲除的小鼠胶质母细胞瘤肿瘤Zpf36l1显著增加生存的动物的时候了。”
单细胞转录组
研究人员利用单细胞转录组为基础的研究。这允许他们识别和比较,所有的RNA分子在每个开发大脑神经胶质细胞和发展恶性胶质母细胞瘤细胞。这包括不同的人口过渡少突细胞和星形胶质细胞的祖细胞,特别是早期pri-OPC祖细胞,胶质母细胞瘤的快速增长提供支持。
之前研究人员称,这项研究很重要,因为新技术的发展使单细胞分析,极其多样化遗传学和类型的脑细胞,导致高档胶质母细胞瘤很难确定。
来确定他们的观察小鼠神经胶质瘤模型可能适用于人类大脑肿瘤的肿瘤形成,研究人员分析了单细胞转录组的人类肿瘤细胞捐赠的病人。他们发现类似的人口和人类少突细胞祖细胞基因签名。细胞已经退化到欠发达有丝分裂状态,认为快速增长的茎状的大脑细胞的特点,为肿瘤发生。
临床前研究正在进行
研究人员强调他们的数据是在实验室老鼠和其他脑癌的模型,所以它仍然是未知的结果是否会转化为病人治疗。研究并提供重要的线索,然而,在抗击癌症通常是致命的,包括儿童,研究人员说。
现在鲁和他的同事们知道阻止Zfp36l1函数在神经胶质瘤细胞形成原始少突细胞祖细胞抑制胶质母细胞瘤生长在实验室模型,他们扩大他们的努力。他们想要找到一个有效的方法治疗利用他们所认为是一个潜在的新漏洞的疾病,到目前为止不可战胜。这包括未来的工作发展特定的治疗药物,可能更准确和有效地目标Zfp36l1和大脑细胞它帮助癌变。