发现的一个主机信使rna抑制免疫功能,抗病毒蛋白质rig - i
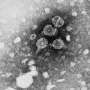
丙型肝炎病毒(HCV)是一个hepatotropic病毒,全球约有8000万慢性感染证实。丙肝病毒感染会导致慢性肝炎的发展,肝硬化,和在某些情况下,肝细胞癌。最近发展的高度有效的直接的抗病毒药物(DAAs),针对病毒蛋白,促进病毒消除> 90%的个体对待。然而,DAA失败的机制在剩下的10%是不理解。
肝脏是一个重要器官的功能代谢碳水化合物,蛋白质和脂肪,清除毒素和病原体,免疫反应的调节。以前,现在的研究小组发现硒蛋白P(9月),一个liver-derived分泌蛋白;他们报告说,9月的感应胰岛素抵抗并参与了2型糖尿病的发病机制。有趣的是,两个患者慢性肝炎C (CHC)和2型糖尿病倾向于DAAs反应迟钝。在目前的研究中,该组织调查感染丙肝病毒的致病性和临床关系和2型糖尿病,专注于9月。
金泽大学组调查9月在抗病毒免疫反应的影响肝脏,使用培养的细胞、老鼠和临床标本。他们发现丙肝病毒感染增强9月培养细胞中表达。通过分析临床样本,他们发现,在hcv感染患者血清9月水平高于健康对照组,按实际使用量付费,治疗更有效的患者更高水平的9月的表情。
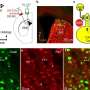
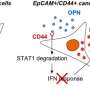
另一方面,一个了不起的镇压与抑制丙肝病毒复制培养细胞中可观察到9月的表情。这些细胞也发现一个增广干扰素(IFN)的生产,具有抗病毒活性。人类是已知有一个系统来检测病毒入侵细胞,诱导干扰素生产。rig - i和MDA5(黑色素瘤differentiation-associated基因5)识别virus-derived RNA和诱导干扰素生产。尽管rig - i和MDA5有高度同源的解旋酶域,他们认识到不同的RNA根据RNA结构,以及基本对齐(PAMP时:其分子模式)。丙肝病毒被认为是由rig - i和MDA5辨认。通过执行实验使用rig - i基因敲除细胞系和MDA5淘汰赛细胞系,9月被发现专门规范rig - i pathway-dependent先天免疫反应。
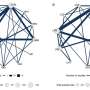
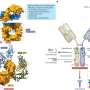
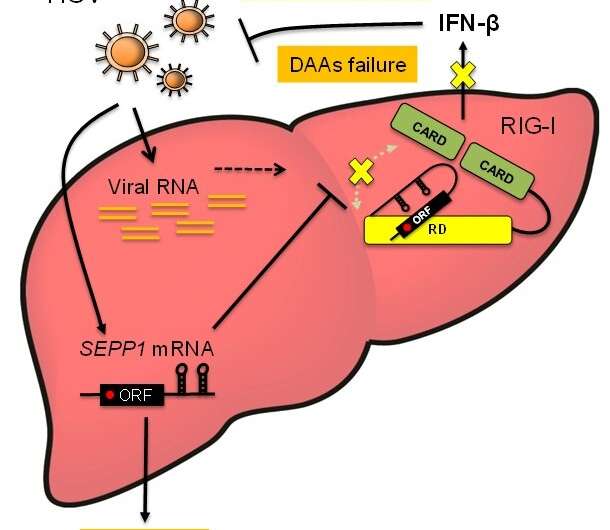
在更详细的实验中使用纯化SeP和合成RNA,镇压先天免疫的9月是显示不是蛋白质,而是9月带来的mRNA。在绑定rig - i的病毒RNA, rig - i的腺苷三磷酸酶活动刺激诱导three-demensional结构性变化和寡聚化rig - i,这与线粒体结合抗病毒信号蛋白激活干扰素生产。9月发现过度的信使rna抑制腺苷三磷酸酶活动重要rig - i激活步骤:寡聚化rig - i和rig - i本地化的线粒体。9月信使RNA,通过绑定和监管领域相互作用(RD) rig - i专门识别和捕捉病毒RNA,蛋白质抑制rig - i激活所需的三维结构改变,和消极监管先天免疫。
因此本研究阐明先天免疫的调节机制通过rig - i SeP mRNA,抗病毒的免疫调节机制在肝脏。
因为慢性丙型肝炎和2型糖尿病高发病率在世界范围内,他们必须尽早治疗。在这项研究中,我们调查了临床丙肝病毒感染和2型糖尿病之间的关系,关注9月,胰岛素抵抗的诱导物。rig - i蛋白被认为只有认识到rna的病原体入侵细胞从而防止病原体,而不是按照主机rna。到目前为止,很少有主机mRNA已报告像9月mRNA,哪些功能作为“诱饵”绑定rig - i从而抑制其功能。这些信息是重要的,对于理解免疫耐受在肝脏和自身免疫性疾病。研究预计将导致进一步的调查主机rna调节rig - i和临床应用的发展,针对这样的mrna,如核酸药物。
这项研究发表在细胞宿主和微生物。
更多信息:细胞宿主和微生物(2019)。DOI: 10.1016 / j.chom.2019.02.015