研究人员识别黑色瘤中BRAF抑制剂的抵抗机制
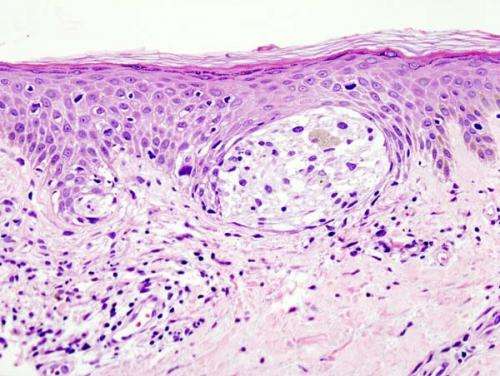
黑色素瘤是一种最具侵袭性的皮肤癌,但最近靶向治疗的进展已经改善了许多患者的预后。不幸的是,对于一些患者来说,这些积极的结果并不持久,因为出现了耐药性和肿瘤复发。莫菲特癌症中心的研究人员发现,黑色素瘤细胞对针对BRAF蛋白及其信号通路的常用药物产生耐药性的机制。该杂志今天在网上发表了他们的研究癌症研究。
黑色素瘤中最常见的遗传突变之一是BRAF基因的改变。BRAF中的突变在大约50%的黑色素瘤中发现,导致增加细胞增殖和生存。有几种药物可用于目标BRAF和名叫MEK的下游基因与癌症发展中的BRAF合作。这些药物导致患者结果的显着改善;然而,许多患者最终发展耐药性。
Moffitt研究人员进行了一系列实验室实验细胞系和小鼠模型,以确定黑素瘤如何抵抗这些常用的药物。他们发现了黑色素瘤细胞对BRAF抑制剂耐药的细胞,其反应机制与受到应激诱导因素(如紫外线辐射和低氧)处理的细胞类似。在这些条件下,细胞增加了蛋白组蛋白去乙酰化酶8 (HDAC8)的表达。
HDAC是调节细胞内其他蛋白质的表达水平和活性的蛋白质。HDAC常规于癌症和几种靶向HDAC的药物被批准用于治疗不同类型的癌症。研究人员发现,HDAC8刺激了AP-1转录因子的活性,随后增加了参与细胞运动和侵袭的基因的表达。
Keiran Smalley博士解释说:“我们的工作提供了第一个证据,表明HDAC8的活性在应对多种多样的细胞压力时增加,这反过来又启动了一个转录程序,该程序与增加黑素瘤细胞存活有关。”莫菲特唐纳德·a·亚当斯黑色素瘤和皮肤癌卓越中心主任。
HDAC8和耐药性之间的这种联系向研究人员表明,靶向HDACs的药物可能能够克服对BRAF抑制剂的细胞耐药性机制。研究人员对小鼠进行了一系列实验,发现HDAC和BRAF抑制剂联合治疗比单独使用任何一种药物更能抑制黑色素瘤的生长。
研究人员希望他们的工作将导致临床研究,将检查HDAC抑制剂的潜力,以防止黑色素瘤耐药性的发展。Smalley说:“这些发现为开发更有选择性和更强效的HDAC8抑制剂提供了强有力的理论基础,以供未来评估,作为限制黑色素瘤表型转换和治疗逃逸的药物。”












用户评论