最常见的研究揭示了如何注定ALS突变细胞

圣裘德儿童研究医院的科学家已经破解神秘最常见的肌萎缩性脊髓侧索硬化症(ALS)的遗传原因,或卢伽雷氏症。研究表明可能致命的疾病的诊断和治疗的新方法。今天在线研究结果刊登在《华尔街日报》分子细胞。
大约35%的ALS与突变基因C9orf72相关病例,使其最常见的肌萎缩性侧索硬化症,另一个神经系统疾病的遗传原因,额颞叶痴呆(FTD)。突变会导致显著增加短的重复DNA序列的数量和结果在不同长度的重复异常蛋白质的形成。这些蛋白质被称为二肽重复多肽(dpr)形成的两个dpr含有氨基酸精氨酸,并特别有毒的神经元。
直到现在,关键细节的分子机制是不确定的。
“我们已经确定了蛋白质、nucleophosmin DPR的毒性,“说通讯作者理查德•Kriwacki博士,圣裘德的成员结构生物学。“我们还表明,DPR毒性极其长度的依赖。在未来,DPR长度可能为诊断ALS患者预后价值。”
肌萎缩性侧索硬化症,dpr和疾病
ALS是一个快速进行性神经系统疾病,杀死神经细胞负责自愿肌肉控制。额颞叶痴呆造成的损失神经细胞在大脑中。目前没有治愈疾病。
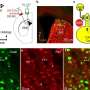
通常,一段C9orf72基因重复20到30次或更少。然而,这些与ALS和FTD成百上千的重复,然后导致dpr的形成。先前的研究从Kriwacki和其他有毒(arginine-containing)报道,dpr扰乱核仁的组装和功能,最大的membrane-less细胞器的细胞。这项研究强调了他们如何扰乱核仁的组装。研究还表明,长dpr细胞显著毒性更强。
核仁驻留在细胞核和细胞的蛋白质工厂(称为核糖体)组装。与细胞核、核仁缺乏一个膜。Membrane-less细胞器如核仁依赖这一过程被称为液-液分离形成阶段,给细胞灵活地应对不断变化的环境。相同的过程解释了为什么石油形成的水滴。
不请自来的客人
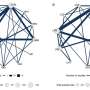
Kriwacki和他的同事们展示了有毒dpr扰乱细胞功能紧密结合nucleophosmin的关键区域,取代其他具有约束力的合作伙伴,帮助维持核仁和核糖体的组装。有毒dpr的浓度越大,越快membrane-less核仁是改变和溶解。
dpr绑定和隔离nucleophosmin内大的复合物,导致细胞核部分溶解。研究显示,有毒dpr也破坏了细胞的功能绑定和隔离ribosomes-ribosomal rna的一个关键组成部分。
核磁共振
一个1.1 GHz核磁共振(核磁共振)系统安装计划于今年晚些时候在圣裘德固化的结果,Kriwacki说。制造商的设备,目前苏黎世瑞士,拥有世界上最强大的高分辨率核磁共振磁体加强生物样本的研究。研究人员使用它在这项研究中更详细地揭示有毒nucleophosmin dpr绑定到内在无序地区。
临床的可能性
“工作还提供了一个新的方向思考可能的治疗目标有毒dpr和他们的网站在病人的行动细胞第一作者迈克尔·怀特说:“博士,博士后Kriwacki的实验室。
“成功将完全创新方法,”Kriwacki说。“但至少现在我们知道需要的目标。”
更多信息:迈克尔·r·白et al, C9orf72保利(PR)二肽重复干扰生物分子相分离,破坏核仁的功能,分子细胞(2019)。DOI: 10.1016 / j.molcel.2019.03.019