研究人员发现了杀伤肿瘤的免疫细胞如何攻击活小鼠的淋巴瘤

这项研究将于4月1日发表在实验医学杂志来自巴斯德研究所和INSERM的研究人员揭示,嵌合抗原受体(CAR) T细胞可以通过直接靶向和杀死癌细胞来诱导肿瘤消退,揭示了这些免疫细胞如何工作的新细节,以及如何提高它们在治疗非霍奇金淋巴瘤和其他B细胞癌症中的有效性。
CAR - T细胞是基因工程的免疫细胞可以专门用来攻击病人的肿瘤细胞.例如,CAR - T细胞靶向一种名为CD19的蛋白质,这种蛋白质存在于许多淋巴瘤和白血病细胞上,是fda批准的几种B细胞恶性肿瘤的治疗方法,包括非霍奇金淋巴瘤和急性淋巴细胞白血病。
然而,一些患者对抗CD19 CAR - T细胞没有反应,而另一些患者在初步改善后,复发并发展出不再表达CD19的耐药肿瘤。巴斯德研究所的Philippe Bousso及其同事认为,改善治疗的关键是更多地了解CAR - T细胞是如何工作的。例如,目前尚不清楚CAR - T细胞是否能杀死癌细胞癌症细胞还是诱导其他免疫细胞攻击肿瘤.
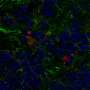
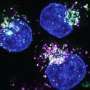
在这项研究中,研究人员追踪了注射到B细胞淋巴瘤小鼠体内的抗cd19 CAR - T细胞的活性。使用一种被称为活体双光子成像的显微镜技术,Bousso和同事们能够看到单个CAR - T细胞杀死动物骨髓中的淋巴瘤细胞。一些CAR - T细胞似乎比其他细胞更活跃,但在大多数情况下,淋巴瘤细胞在与CAR - T细胞直接接触后几分钟内死亡。这表明CAR - T细胞主要是直接杀死它们的目标。
Bousso说:“基于我们实验数据的计算机模拟支持这样一种观点,即CAR - T细胞依赖于它们直接的细胞毒活性,而不是招募和激活其他细胞来消除骨髓中的大部分B细胞淋巴瘤。”
模拟还表明,CAR - T细胞渗入骨髓的相对微小差异可以对治疗结果产生重大影响。CAR - T细胞无法渗透骨髓的一个原因是,如果它们遇到在血液中循环的淋巴瘤细胞,或者也表达CD19的健康B细胞。Bousso和同事们发现CAR - T细胞可以与这些循环细胞聚集在一起,并被困在肺部,阻止它们到达骨髓。减少这些相遇——例如,通过暂时减少循环B细胞的数量——增强了CAR - T细胞渗入骨髓并杀死肿瘤细胞的能力,延长了B细胞淋巴瘤小鼠的生存时间。
Bousso说:“因此,在CAR - T细胞移植前清除循环肿瘤细胞和正常B细胞可能通过改善CAR - T细胞的植入和持久性而提供临床益处。”
尽管如此,研究人员发现肿瘤复发和缺乏CD19的肿瘤的出现发生在骨髓而不是在其他受B细胞淋巴瘤影响的器官,如淋巴结。这似乎是因为CAR - T细胞在这些其他器官中不那么活跃,降低了肿瘤的诱因细胞从而失去CD19蛋白
“总之,我们的研究结果揭示了CAR - T细胞在影响植入、抗肿瘤活性和肿瘤复发的不同解剖部位的行为的巨大多样性,”Bousso说。“了解这些差异是开发优化CAR - T细胞治疗策略的重要一步。”