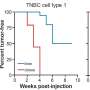
如何饿死三阴性乳腺癌
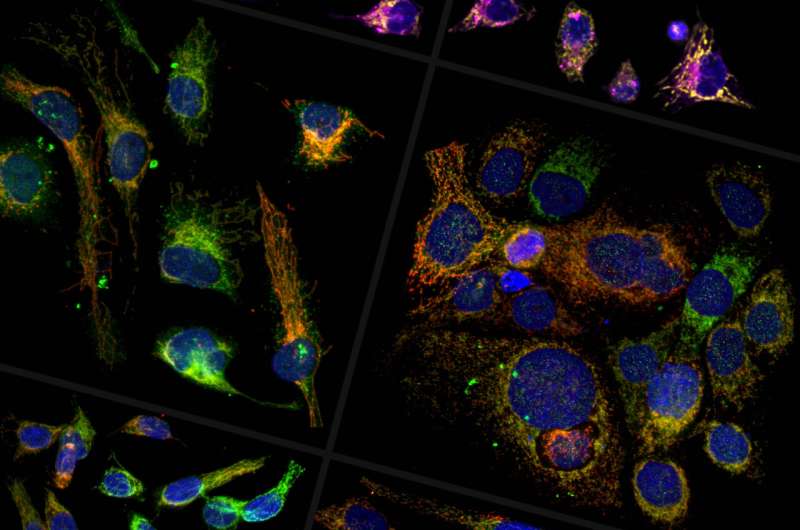
巴西的一个研究小组已经开发出一种策略,慢三阴性乳腺癌细胞的生长通过削减他们从两个主要的食物来源。
三阴乳腺癌或TNBC占大约15%到20%的乳腺癌和在非裔美国妇女最常见。这些肿瘤缺乏雌激素和孕激素受体和HER2蛋白存在于其他乳腺癌并允许特定的靶向治疗。因为每个TNBC肿瘤都有不同的基因构成,寻找新的标记,可以指导治疗一直是一个艰巨的任务。
“有强烈的兴趣,寻找新的药物可以治疗这种乳房癌症桑德拉玛莎说:“戈麦斯迪亚斯,癌症研究员巴西坎皮纳斯生物科学国家实验室,巴西。“TNBC被认为是更积极,比其他类型的乳腺癌预后较差,主要是因为很少有针对性的药物治疗TNBC。”
在一项新的研究生物化学杂志,迪亚斯和他的同事们证明除了谷氨酰胺,一个著名的癌症的食物来源,TNBC细胞可以使用脂肪酸成长和生存。当抑制剂阻止谷氨酰胺和脂肪酸代谢被用于音乐会,TNBC增长和迁移放缓,迪亚斯说。
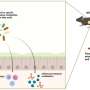
保持他们飞速增长的能力,癌症细胞消耗营养物质的速度增加。谷氨酰胺,这是最丰富的氨基酸在等离子体就是其中之一。某些类型的癌症成为严重依赖这个多功能分子提供能源、碳、氮、和抗氧化性能,所有这些支持肿瘤细胞的生长和生存,迪亚斯说。
药物Telaglenastat,也称为cb - 839,阻止了谷氨酰胺的处理,目前正在临床试验治疗TNBC和其他肿瘤类型。cb - 839的作品去活化酶谷氨酰胺酶,阻止肿瘤细胞分解和收获谷氨酰胺的好处。然而,最近的研究表明,一些TNBC细胞可以抵抗的药物治疗。
看看这些细胞基因表达的改变可以解释如何生存,这项研究的作者暴露TNBC细胞cb - 839定义那些抵抗,那些敏感的药物,并测序RNA,迪亚斯说。
在耐药细胞,分子途径处理相关的脂质高度改变,迪亚斯说。特别是,水平的酶CPT1 CPT2,脂肪酸代谢的关键,是增加。
“CPT1和2作为网关入口的脂肪酸进入线粒体,在那里他们将被用作燃料的能源生产、“迪亚斯说。“我们的假设是,关闭这个网关通过抑制CPT1结合谷氨酰胺酶抑制作用会降低经济增长和耐迁移cb - 839 TNBC细胞。”
双重抑制证明意义重大,因为它减缓耐药TNBC增殖和迁移细胞多个人CPT1或谷氨酰胺酶的抑制。这些结果提供新的遗传标记,能够更好地指导药物选择TNBC患者,迪亚斯说。
进一步探索