研究人员发现阻止视网膜再生机制

发现打开一天恢复视力丧失的可能性通过激活视网膜再生的能力。休斯顿贝勒医学院的研究人员医学、心血管研究所和德克萨斯心脏研究所揭示杂志上细胞的报道,虽然专业的哺乳动物retina-a层神经细胞介导愿景和位于眼睛后面的——不自发再生,再生能力,保持休眠的细胞称为河马通路的机制。发现打开的可能性激活视网膜的能力恢复失去的愿景通过操纵这个途径。
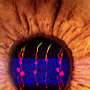
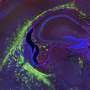
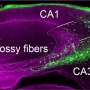
“损害视网膜视力会导致不可挽回的损失在人类和其他哺乳动物,因为他们的视网膜不再生,”主要作者罗斯博士说a . Poche分子生理学和生物物理学和助理教授丹•邓肯L综合癌症中心的成员贝勒。“然而,斑马鱼可以扭转失明等其他动物由于特殊细胞在视网膜上称为穆勒神经胶质细胞。当视网膜受损,穆勒胶质细胞增殖和分化成丢失视网膜神经元,有效地取代受伤的细胞功能齐全的。”
尽管穆勒在受伤的哺乳动物的视网膜神经胶质细胞不恢复视觉作为他们的同行在斑马鱼,其他研究人员已经表明,哺乳动物的视网膜受损时,穆勒胶质细胞的一个小子集的第一步需要进入增殖周期,如获取分子标记科学家预计在增殖细胞。
“但这企图增殖是短暂的;收购后的一些细胞标记细胞关闭,“Poche说,他也隶属于智力和发育障碍研究中心和卡伦眼科研究所,贝勒。“这些观察表明,导致斑马鱼细胞修复的机制也可能存在于哺乳动物,但它是积极抑制。多年来,抑制机制尚不清楚。”
寻找拟议中的抑制机制,Poche实验室联合共同通讯作者詹姆斯·马丁博士的实验室,分子生理学和生物物理学教授,维维安·l·史密斯椅子在再生医学贝勒医学院和心肌细胞更新实验室主任德州心脏研究所。研究人员将注意力集中到了河马通路网络的分子事件,导致器官增长在发展和监管的心肌梗死心脏组织再生反应。马丁实验室先前表明,河马通路就像一个“突破”在心肌细胞增殖抑制活性的另一个途径称为狂吠。
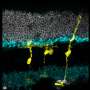
在这项研究中,研究人员首先确定河马通路穆勒哺乳动物神经胶质细胞中表达。然后,他们研究了改变河马途径在这些细胞是否会影响其增殖能力。创建一个故障河马通路通过消除两个分子的步骤导致细胞增殖。当研究者转基因穆勒胶质细胞携带的一个版本YAP称YAP5SA不受河马的抑制性影响,显示主要的增殖和细胞祖细胞的身份。重要的是,其中的一个小子集穆勒glia-derived祖细胞表现出自发分化成新的视网膜神经元的迹象。
“到目前为止研究人员不知道内生阻塞机制阻止Muller细胞进入再生状态。河马通路是一种新的分子机制的入口点,“Poche说。“我们的下一步是开发一个战略指导增殖Muller视网膜神经胶质细胞分化途径细胞可以恢复视力。”
更多信息:细胞的报道(2019)。DOI: 10.1016 / j.celrep.2019.04.047