更好地理解冯·维勒布兰德因子A2域
在正常,健康的循环条件下,血管性血友病因子(vWF)保持自己。巨大而神秘的多聚体糖蛋白在血液中移动,紧紧地缩成一团,它的反应部位没有暴露出来。但当大量出血发生时,它就会开始行动,启动凝血过程。
当它正常工作时,vWF有助于止血和挽救生命。然而,世界上大约1%到2%的人口受到vWF突变的影响,从而导致出血性疾病。对于那些更罕见、更严重的形式,可能需要一种非常昂贵的血浆置换形式的治疗。
另一方面,如果vWF在不需要它的地方激活,就会引发中风或心脏病发作。
更好地了解vWF的功能可能会导致药物替代那些缺乏vWF的人。这也可能导致新的药物或药物载体的开发,模仿蛋白质的行为,以更有效的药物输送。
考虑到这一点,里海大学的一组研究人员正在研究这种神秘蛋白质的特征。在最近发表于生物物理期刊,他们利用微流控装置和荧光显微镜,为vWF的剪切诱导伸展响应提供了实验数据。此外,他们使用实验参数化粗粒度VWF模型的串联布朗动力学模拟结果来帮助解释他们从实验中得到的一些中心观测结果。这项工作进一步阐明了栓系VWF的流诱导生物力学响应行为的细节,并展示了与实验相结合的日益复杂的粗粒度模型的力量和能力。
这篇论文名为“Tethered von Willebrand Factor的剪切诱导拉伸响应行为”,作者是材料科学与工程副教授宣宏Cheng;机械工程和力学教授Alparslan Oztekin;埃德蒙·韦伯三世,机械工程和力学副教授;生物工程、机械工程和力学副教授Frank Zhang;以及博士生Michael Morabito和Yi Wang。
vWF在工作
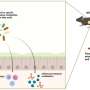
在一个小伤口的位置,血小板粘附在靠近血管壁孔洞的胶原蛋白暴露部位,起到堵塞的作用,有效止血。快速血液流动然而,这使得血小板很难做到这一点。幸运的是,冯·维勒布兰德因子能识别这种快速的血液流动并激活:“如果你愿意的话,这是一个由流动机制激活的事件,”韦伯解释说。
球状分子像弹簧狗一样展开,伸展到原来的10倍大,并暴露出它的反应网站.它附着在破裂的血管壁上,在那里暴露的胶原蛋白(血管壁上的结构蛋白)吸引血小板。然后vWF从血液中捕获血小板,就像胶原蛋白和血小板之间的桥梁一样。
虽然vWF的生物学功能早已被科学家们所认识,但人们对vWF的具体功能知之甚少,特别是在流动条件下。
Cheng说:“血液功能中的大多数蛋白质是通过生化反应执行的。”“这种蛋白质(vWF)也需要一些生化反应来发挥其功能,所以它需要抓住血小板,抓住胶原蛋白——这些都是生化反应。同时,vWF依靠机械刺激来执行生化功能,这部分并不为人所知。这就是我们正在努力研究的。”
韦伯补充说:“来自我们小组和其他小组的一些数据表明,这些生化反应在某种程度上受到某种张力和拉力的刺激。因此,即使是生化反应似乎也在某种程度上是机械介导的。再一次,我们可以理解,从一个紧凑的,几乎像球一样的形状,变成了这个长而细的东西。但最近有人指出,不仅仅是这样。为了使这个化学位点活跃,你必须拉它,你必须在局部有一点张力。所以这是一个非常迷人的系统。”
解开A2
冯·维勒布兰德因子是一种特别大的蛋白质,由许多单体或可以与其他相同分子结合形成聚合物的分子组成。在vWF的每个单体中都有不同的域:A、C和d。每个域及其各自的子域都有自己的角色,其中许多角色还不为人所知。例如,A1结构域将vWF与血小板结合。A3绑定vWF到胶原蛋白.A2结构域展开以暴露蛋白质的反应位点,当完全打开时,暴露一个允许vWF分子分裂到一定大小的位点。团队成员特别关注A2领域。
Oztekin说:“我认为,理解这个领域以及它如何与流程相互作用是我们团队的最佳贡献。”
团队中的每个成员都扮演着特定的角色。程,张和他们的研究生在项目的实验方面工作;Oztekin, Webb和他们的研究生专注于模拟。每个团队的结果都是另一个团队工作的依据。
张教授多年来一直在研究vWF,并将该项目带到了里海大学,他擅长单分子力谱学和机械感测,即细胞如何对机械刺激做出反应。他使用一种叫做光镊子的专门工具,这种工具利用聚焦的激光束对小到单个原子的物体施加力。
“光学镊子可以抓取微小的物体,”张解释道。“我们可以抓住vWF,同时我们施加力,看看蛋白质是如何改变形状的,看看蛋白质是如何在有机械扰动或机械力时被激活的。”
程的发展微流体装置,其直径较小,可用于分析活的生物制品。她和她的团队制造了非常小的类似于血管几何形状的通道——大约10微米高,几毫米长和宽——这样他们就可以模拟vWF在体内遇到的流动条件。他们用荧光标记vWF分子,并使用共聚焦显微镜捕捉分子以不同速率流过通道时的视频和静态图像。
Cheng解释说:“当我们谈论正常流动下的这种蛋白质时,它是一种构象,然后当它暴露在某些异常流动模式下时,你会有不同的构象。”“所以我们试图在体外系统中描述或复制这一过程,试图观察这种蛋白质在不同的流动模式下如何改变构象。然后,如果我们有突变体和正常蛋白质,它们会有什么不同?”
博士生王毅(Yi Wang)与程教授在微流体通道上合作,他们可以在显微镜下实时观察vWF分子的展开和折叠。要做到这一点,他们必须创造一个环境,模仿剪切速率,或血液流动速度的变化,在体内发现。
王说:“因为我们使用了相当高的剪切速率来与生理环境相比较,而且由于成像分子的显微镜镜头的移动速度有限,如果分子在运动,那么捕捉它的运动实际上是相当具有挑战性的。”
为了解决这个问题,研究小组将分子的一侧与通道表面结合,在施加剪切力时使其固定。他们成功地用视频捕捉到了这一正在展开的现象。
“如果它(分子)束缚得太紧,它就会停留在那里(而不会展开),”王说。“如果太松,所有东西都会被冲走。所以当我们找到了将它绑定在表面上的最佳位置,这样它就可以展开和折叠时,我非常兴奋。”
进一步探索