新研究将氧化应激与异常蛋白质的扩散
氧化应激可能是扩散的驱动力异常蛋白质参与帕金森病。这是实验室研究的结果德国中心的研究人员对神经退行性疾病(DZNE)。研究结果发表在“临床研究杂志”。
帕金森氏症是一种神经退行性疾病与临床表现,包括汽车(如地震和缓慢运动)以及非机动车(如睡眠障碍和抑郁)的症状。在微观和病理水平,这种疾病的特点是异常积累intraneuronal夹杂物。他们是由于聚合形成的蛋白质被称为“α-突触核蛋白”。在疾病过程中,这些夹杂物逐渐出现在不同的大脑区域,导致逐渐恶化的疾病严重程度。这背后的机制促进病理学是知之甚少。现在DZNE科学家的研究表明,“氧化应激”,即过度和不受控制的活性氧的生产,可以发挥重要的作用在α-突触核蛋白的病态蔓延。研究结果是基于已与老鼠和体外培养细胞实验研究。
“氧化压力长期以来一直被认为是参与帕金森病的发病机制。然而,我们的工作就会发现一个新的有趣的机制,可能与氧化应激对疾病的发展。我们表明在氧化应激α-突触核蛋白的倾向“旅行”从一个神经元到另一显著增强,从而促进交换的有害蛋白质种类、发生的病理学和病理的传播在整个大脑,“高级DZNE Donato迪蒙特教授说科学家,他当前的研究。
他补充说,“虽然在我们的研究中我们在实验室人工诱导氧化应激模型,我们知道增加产量的有害的氧物种可能发生在帕金森病的大脑。它可能引起的各种条件,如基因突变和环境因素可能与衰老过程本身的细胞机制抵消氧化压力随着年龄的增长而下降。帕金森氏症是一种与年龄相关的疾病,很有可能,老化的大脑细胞将成为更容易涉及氧化应激的病理过程。”
实验设置
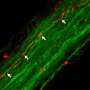
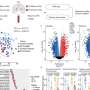
在一系列的实验中,迪蒙和他的同事们研究了小鼠过度生产α-突触核蛋白在一个特定的大脑区域,即背延髓,已知α-突触核蛋白在帕金森病病理学的主要目标。在这种情况下,研究人员能够显示氧化应激,形成小的α-突触核蛋白聚集(所谓的低聚物)和神经损伤。增加生产α-突触核蛋白也导致其“跳”从供体延髓成神经元受体神经元在邻近的大脑区域,成为影响进步的α-突触核蛋白聚集和聚合。治疗百草枯的老鼠,有趣的是,一种化学剂,产生大量的活性氧,从而引发氧化应激,加剧了α-突触核蛋白病理学并导致其更加明显蔓延在整个大脑。
“我们的研究结果支持假设可能引发的恶性循环α-突触核蛋白负担和氧化应激增加,”迪蒙说。“氧化应激可以促进α-突触核蛋白聚集形成的,反过来,可能加剧氧化应激。跳从一个神经元传到另一个神经元,这种有毒的过程可能影响越来越多大脑地区和有助于进步病理学和神经元死亡。”
异常蛋白质
α-突触核蛋白的确切机制增强神经元传递下氧化应激并不完全理解。然而,迪蒙和他的同事们更详细的分析,包括体外实验,揭示形成和积累的形式的α-突触核蛋白异常氧化和硝化氧化应激的结果。这些异常蛋白质的物种被发现特别是移动和更容易从供体受体细胞。
“识别有毒α-突触核蛋白的物种倾向高聚合和传播有重大影响,”迪蒙说。“他们可能会成为治疗干预的目标,可以预防疾病早期发育和/或抵消疾病后期的病理学的发展。”
更多信息:露丝·e·Musgrove et al,氧化应激在迷走神经的神经元促进帕金森病理学和细胞间α-synuclein转移,临床研究杂志(2019)。DOI: 10.1172 / JCI127330