血栓在血流中是如何变硬的?一种新的工程组织模型给出了答案
血液凝固是人体生理中最重要的保护性过程之一。当凝血出现问题时,要么是因为凝血过多导致中风,要么是因为凝血不足导致内出血,结果可能是灾难性的。
现在,布法罗大学的研究人员已经建立了这一过程的体外模型,这将帮助临床医生改善某些出血性疾病患者的术前计划和护理,特别是血小板缺陷血细胞会形成血栓)和影响患者形成血栓能力的因素。这项工作也为血小板和血液之间可能发生的变化提供了一幅图景血管有前所未有的细节。
五月出版于自然通讯,这篇论文揭示了UB生物工程师构建的模型如何模拟何时发生的复杂性血凝块在受伤的地方。
剪切应力
血液流动和血管壁上的剪切应力血容器是很大的因素心血管系统赵若刚博士说,他是这篇论文的通讯作者,也是生物医学工程系的助理教授,生物医学工程系是布法罗大学工程与应用科学学院和雅各布斯医学和生物医学科学学院的一个联合部门。他与布法罗大学其他院系的研究人员合作,包括共同通讯作者、化学和生物工程教授Sriram Neelamegham博士。
在进行手术之前,外科医生需要了解患者的出血史和血液凝块能力。治疗各种血液疾病的血液学家还需要了解具体的治疗方法如何改变患者形成血栓的能力。目前,有一些设备可以用于临床和家庭护理环境,以帮助表征患者的血凝块。
但是,赵指出,这些设备缺乏实际模拟凝块如何形成以及剪切流动如何影响凝块的能力,这限制了它们的实用性。他解释说剪切应力是血液流动对血管壁的作用力的结果,类似于水在房子里流经管道的方式,随着时间的推移,对这些管道施加力和压力。
“在过去的几十年里,我们已经知道沿血管壁的剪切力会影响血小板附着在受伤部位的方式,”Zhao说,“但我们还不清楚这是如何影响凝血过程和结果的。”
“这很重要,因为正常的凝血直接依赖于凝块的硬度,”他说。“如果血块太软,它就会被冲走。如果太硬,就会形成血栓,阻碍血液流动,并可能导致中风和心脏病等并发症。”
在血液流动的剪切力存在的情况下,保持这种微妙的平衡变得更具挑战性。
赵医生说,血小板是一种非常聪明的凝血细胞。如果没有受伤,它们就会安静地循环。但如果它们接触到胶原蛋白,这意味着有损伤,它们就会激活。它们冲向那个地点,但不同的血液流速会改变它们的活动。
对流量和刚度进行建模
“我们系统的创新之处在于,我们可以模拟流动条件和凝块的刚度,这就给出了发生情况的最真实的画面。没有其他模式可以做到这一点。”
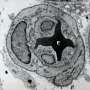
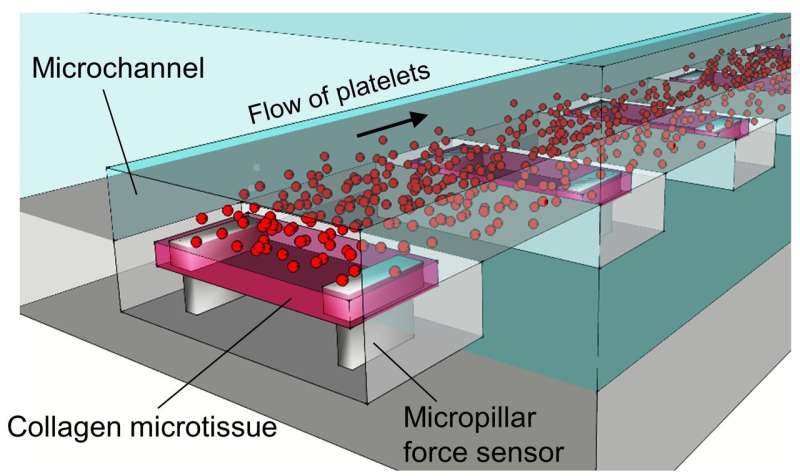
该系统模拟了血小板如何附着在受伤的血管壁上并形成血栓的动态过程,同时提供了关于已经形成的血栓的机械特性的实时信息。因此,它模拟了剪切流动过程中的凝块形成和凝块力学。
Zhao和他的同事们使用微加工技术做到了这一点,创造了机械传感平台,允许同时控制凝块的形成和凝块力学,模拟硬化过程。
UB系统的关键创新是开发了灵活的微柱,可以测量凝块的刚度。
“当血小板附着在微胶原蛋白上时,这些微柱支撑着它,”赵说。“微柱作为力传感器,它们可以感知微凝块的收缩和硬度。没有其他系统可以测量血栓的硬度,因此,它们有多软或多硬。”
他和他的同事开发的模型集成了模拟血管的工程微通道和微柱力传感器,以测量血管的刚度凝块.该系统使用人类志愿者的血液样本进行了测试。
布法罗大学的研究小组使用该设备模拟了遗传出血性疾病患者与正常凝血患者的凝血情况。
该团队计划通过测试更多来自不同凝血障碍患者的样本,进一步验证该系统的临床效用。
进一步探索