CRISPR基因编辑可能停止三阴性乳腺癌的进展
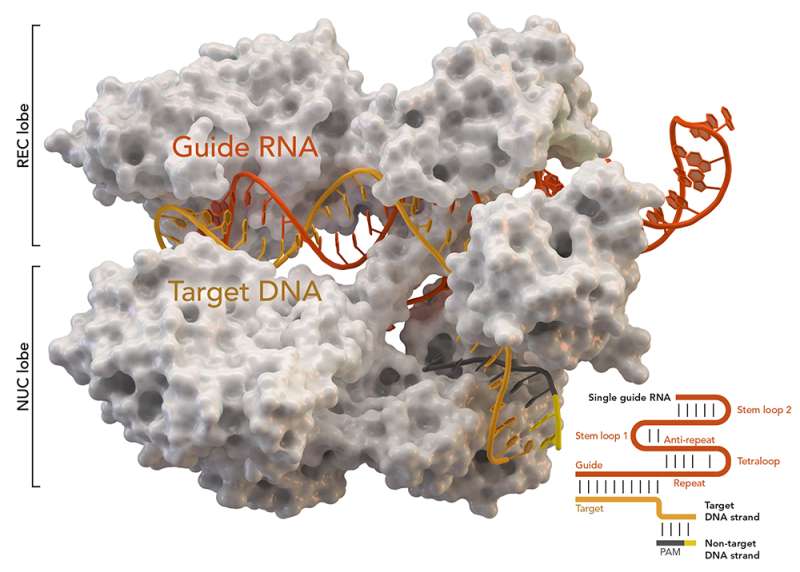
一个tumor-targeted CRISPR基因编辑系统,封装在一个nanogel和注入身体,可以安全有效地阻止三阴性乳腺癌的增长,波士顿儿童医院的研究人员报告。概念验证研究中,在人类肿瘤细胞和小鼠进行的,显示一个潜在的基因治疗三阴乳腺癌的所有乳腺癌的死亡率最高。
新的专利保护策略是在线本周在《华尔街日报》报道PNAS。
三阴乳腺癌(TNBC),缺乏雌激素,孕激素和HER2受体,占12%的乳腺癌。它更频繁地发生在50岁以下的女性,在非裔美国妇女,妇女携带BRCA1基因突变。手术、化疗和放疗的一些治疗方法非常好斗,经常转移性癌症,这是迫切需要更有效的针对性的治疗。
这项新研究中,由彭郭博士和玛莎摩西,博士在波士顿儿童血管生物学程序,代表了首次成功使用目标CRISPR基因编辑停止增长TNBC肿瘤体内(通过注入生活、肿瘤小鼠)。这个新系统是无毒的,利用抗体来选择性地识别癌症细胞,同时保留正常组织。
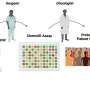
实验表明,CRISPR系统能够在乳腺肿瘤和知名乳腺癌促进基因,Lipocalin 2,编辑效率81%的肿瘤组织。减毒肿瘤生长的方法77%小鼠模型,在正常组织没有毒性。
精确的交付CRISPR
迄今为止,翻译CRISRP基因编辑技术为疾病治疗一直缺乏有效的限制CRISPR交付系统。一个方法使用病毒提供CRISPR系统,但是病毒无法携带大型有效载荷和可能会引起副作用,如果“感染”细胞以外的目标。另一种方法封装了CRISPR系统在阳离子聚合物或脂质纳米粒子,可以对细胞有毒,但这些元素和CRISPR系统经常被困或分解身体才到达目的地。
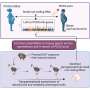
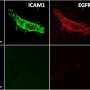
新方法封装了CRISPR编辑系统在一个柔软的脂肪分子“nanolipogel”由无毒,水凝胶。抗体附着在凝胶表面然后指导CRISPR纳米粒子到肿瘤部位。抗体ICAM-1旨在识别和目标,一个分子摩西实验室确认在2014年作为一个新型药物的目标三阴性乳腺癌。
因为粒子的柔软和灵活,他们可以更有效地比硬同行进入细胞。而严厉的纳米粒子可以被细胞摄入机械、软粒子能够与肿瘤细胞膜融合并交付CRISPR载荷直接细胞内。
“用软粒子允许我们更好地穿透肿瘤,没有副作用,和更大的货物,”郭说,这项研究的第一作者。“我们的系统可以大幅提高肿瘤CRISPR交付。”
一旦进入细胞,CRISPR系统淘汰Lipocalin 2,致癌基因,促进乳腺肿瘤进展和转移。实验表明,癌基因抑制的损失癌症的侵略性和迁移或转移的倾向。治疗组没有毒性的证据。
尽管研究集中于三阴乳腺癌摩西认为,团队的CRISPR平台可以适应治疗小儿癌症,也可以提供常规药物。这些研究正在进行。团队与许多公司对技术感兴趣。
“我们的系统可以提供更多药物肿瘤,在一个精确的和安全的方式,“摩西说。
更多信息:彭郭el al。”治疗三阴乳腺癌肿瘤的基因组编辑使用noncationic和变形nanolipogel,”PNAS(2019)。www.pnas.org/cgi/doi/10.1073/pnas.1904697116