单一酶有助于推动炎症小鼠,提供了新的脓毒症药物目标
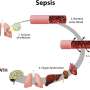
脓毒症时机体沉溺在其试图抵抗感染。免疫细胞冲进去,反应过度,肆虐在组织和器官,经常导致器官衰竭和死亡。
加州大学圣地亚哥医学院的研究人员最近发现,消除酶PHLPP1改善结果的小鼠模型脓毒症。PHLPP1控制许多细胞行为通过消除磷酸盐(小化学标签)与其他蛋白质。现在发现,PHLPP1也影响炎症。
该研究发表8月13日,2019年eLife的可能性,介绍了抑制PHLPP1可能形成人类新的脓毒症治疗的基础。
“大多数研究炎症通常专注于激酶,酶添加磷酸标签其他蛋白质,”资深作者Alexandra牛顿说,博士,教授在加州大学圣地亚哥分校医学院的药理学。“令人激动的是,我们有一个全新的目标sepsis-the酶删除它们。”
牛顿的团队发现PHLPP1几年前已经详细的作用抑制肿瘤。跟踪这些发现,牛顿伸出手来加州大学圣地亚哥分校医学院的同事克里斯•玻璃专家博士炎症。
在一起,他们的团队发现了许多免疫细胞基因受PHLPP1的影响。但PHLPP1的特殊影响炎症可能与事实消除磷酸盐从一个叫做STAT1的转录因子,以控制炎症基因。
牛顿的团队修改了老鼠缺乏PHLPP1基因转移到另一个加州大学圣地亚哥分校医学院的同事,Victor Nizet医学专家细菌感染。在单独的实验中,Nizet的团队管理活细菌和大肠杆菌脂多糖(LPS)的一个组成部分细菌的细胞壁,促使免疫系统野外,PHLPP1-deficient和正常小鼠。
惊讶的牛顿的区别:老鼠没有PHLPP1要好得多。虽然所有正常小鼠死亡侵染诱导的脓毒症后五天,一半的PHLPP1-deficient老鼠活了下来。
牛顿的团队已经与其他合作者合作,筛选数以千计的化合物来识别那些抑制PHLPP1很少。现在他们知道PHLPP1抑制剂可能会形成新的anti-sepsis药物的基础,研究人员希望能测试这些化合物免疫细胞在实验室和在脓毒症小鼠模型。
目前,脓毒症是通过预防和治疗感染源,通常用抗生素,同时保持器官健康与氧气和静脉输液。尽管如此,根据疾病控制和预防中心,在美国至少有170万成年人每年开发败血症,因此,近270000人死亡。三分之一的病人死在医院有败血症。
“败血症死亡的主要原因是在世界各地的重症监护病房,但不幸的是没有一个批准的药物治疗脓毒症,”Nizet说。像我们这样的“发现控制免疫细胞行为的基本信号通路在脓毒症为控制败血症的危险炎症提供线索,同时保留关键的细菌杀死白细胞的属性细胞。"
进一步探索