科学家发现如何在多发性硬化症小鼠模型中阻断炎症分子
你的免疫系统已经准备好与细菌、病毒、真菌甚至癌症作斗争。但在自身免疫性疾病中,免疫系统的超能力会把它变成一个超级反派。现在,索尔克研究所的科学家们发现了一种阻止某些免疫系统细胞错误攻击身体的方法。他们的研究结果于2019年8月26日当周发表在该杂志上美国国家科学院院刊,提出了一种靶向Th17辅助T细胞的新方法。Th17辅助T细胞是一种产生白介素17的免疫细胞,白介素17是一种已知的自身免疫性疾病的根源,如多发性硬化症、类风湿性关节炎和牛皮癣。之前针对Th17辅助T细胞的研究成果有限。
在自身免疫性疾病的情况下免疫系统把武器对准自己,”索尔克NOMIS免疫生物学和微生物发病机制中心的副教授叶正说,他是这项研究的共同高级作者。
“自身免疫性疾病影响大约1 / 30的人。这项研究为治疗这些患者打开了大门,而不会引发有害的副作用,”索尔克基因表达实验室的联合资深作者兼主任罗纳德·埃文斯说,他是分子与发育生物学的March of Dimes主席,也是霍华德·休斯医学研究员。
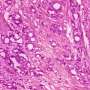
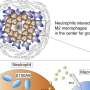
包括第一作者Christina Chang在内的研究团队使用多发性硬化症小鼠模型来研究Th17辅助T中白细胞介素17的过度生产细胞.这些免疫细胞通常用于治疗感染,白细胞介素17发送炎症信号,帮助启动免疫反应。然而,有时免疫细胞变得过度活跃并开始产生过多的白细胞介素17,破坏附近的组织并启动自身免疫性疾病进程。
药物治疗可以减缓白细胞介素17的产生,但它们也可以作为强大的免疫抑制剂,阻断身体对抗感染的整体能力。在这项新研究中,索尔克的科学家们想知道是否有一种方法只阻断白细胞介素17的产生而不损害免疫系统功能。
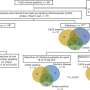
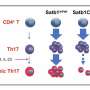
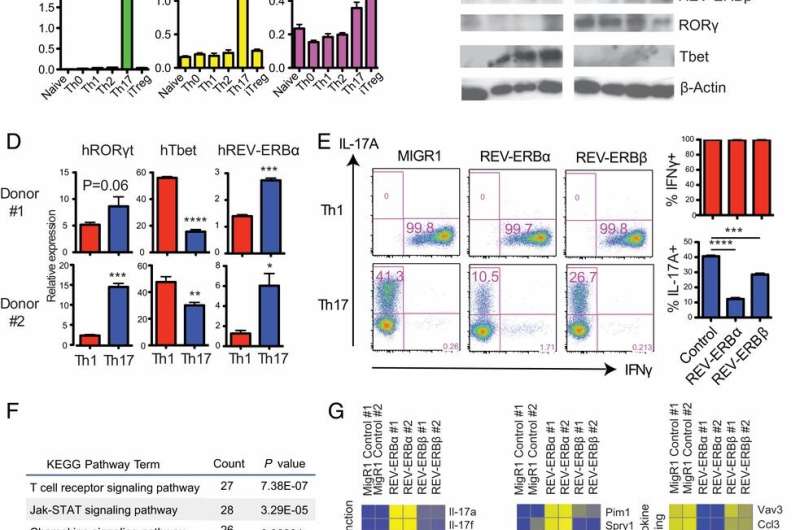
研究小组发现了一种使用REV-ERB分子抑制白细胞介素17产生的方法。REV-ERB与Th17辅助T细胞上的一个位点结合,该位点通常由一种称为ROR的分子占据,负责白介素17的产生。通过接管相同的绑定位置,REV-ERB与ROR竞争。“ROR是驱动这些辅助T细胞的油门踏板,但REV-ERB就像刹车,”郑说。
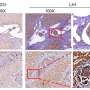
研究人员随后证明,他们能够用化学方法激活REV-ERB,延缓实验性自身免疫性脑脊髓炎(多发性硬化症的小鼠模型)的发病和减缓症状的进展。
还需要做更多的工作,但科学家们表示,针对这一特殊途径提供了一种抑制方法白介素在不影响其他免疫系统的情况下
该研究的合著者、索尔克基因表达实验室的高级科学家迈克尔·唐斯补充说:“这还处于早期阶段,但确实令人鼓舞。”
下一步,科学家们计划研究REV-ERB在类风湿性关节炎和牛皮癣模型中的作用。
更多信息:Christina Chang等人。核受体rev - erba调节Th17细胞介导的自身免疫性疾病,美国国家科学院院刊(2019)。DOI: 10.1073 / pnas.1907563116.www.pnas.org/content/early/201…/26/1907563116.short