药物-光联合疗法可以控制CAR - t细胞疗法
加州大学圣迭戈分校的生物工程师离使CAR - t细胞疗法更安全、更精确、更容易控制又近了一步。他们开发了一种系统,允许他们选择何时何地启动CAR - T细胞,从而在不伤害正常细胞的情况下摧毁癌细胞。
这个系统需要两个“钥匙”——药物它莫西芬和蓝色的光-启动CAR T细胞与它们的目标绑定。只要一个键就可以使细胞处于不活跃状态。研究人员在活细胞培养上测试了他们的系统,作为概念的证明。他们的下一步是在老鼠身上做肿瘤测试。
“有了我们的技术,我们可以更好地控制CAR - t细胞治疗患者,并有可能避免器官和非恶性组织的非特异性靶向,”加州大学圣地亚哥分校生物工程教授Peter Yingxiao Wang说,他是这项研究的资深合著者。研究人员最近发表了他们的研究成果ACS合成生物学。
嵌合抗原受体(CAR) t细胞治疗是一种很有前途的治疗癌症的新方法。它包括收集病人的T细胞,通过基因工程使它们在其表面表达特殊的受体,这种受体可以识别目标抗原癌症细胞。然后将经过改造的T细胞注入患者体内,寻找并攻击表面有靶向抗原的细胞。
这种方法对某些类型的血癌和淋巴瘤很有效。但王解释说,一个主要的问题是,这种方法的效果太好了。许多有针对性的癌症抗原也在表面表达健康的细胞它会导致心脏、肺或肝脏等重要器官受到攻击。这种风险被称为“靶向、非肿瘤毒性”,对接受CAR -t细胞治疗的患者来说可能危及生命。
“传统的CAR - T细胞总是开着的,这意味着它们会持续表达抗原靶向受体。我们的方法是设计T细胞,使其能够在特定的位置和时间范围内选择性地激活表达受体。”
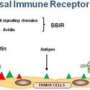
Wang和他的同事们设计了一种T细胞,这种T细胞只在两个输入序列后才被激活:用小分子药物它莫西芬治疗,然后暴露在低强度蓝光短脉冲中。“意外激活的可能性非常低,因为你需要同时输入这两种信息。药物启动细胞,而光线使我们能够精确地引导它们被激活的位置。”王说。
最初,CAR - T细胞处于待机模式。为了启动,两个特定的蛋白质(一个在细胞核外,一个在细胞核内)需要结合在一起,从而触发抗原靶向受体的表达。药物它莫西芬首先与这些蛋白质中的一种结合,帮助它进入细胞核,其他蛋白质在那里等待。然后蓝光诱导这两种蛋白质结合。任何经过药物处理但未暴露在蓝光下的细胞都保持待机模式。
光线不能穿透身体深处,因此王设想这种方法可以用于治疗皮肤、头部和颈部的癌症。他现在正在寻求与临床医生合作在活的有机体内治疗黑色素瘤的试验。
进一步探索











用户评论