基因治疗杜氏肌萎缩症安全地保存肌肉功能

宾夕法尼亚大学医学正在研制一种基因疗法治疗杜氏肌肉营养不良症(DMD)成功地和安全地停止相关的严重的肌肉恶化罕见的基因疾病在这两个小型和大型动物模型,根据首开先河的研究中从宾夕法尼亚大学医学研究人员。结果,今天在线发表自然医学,把领域内的一个安全有效的基因治疗,使用“替代”蛋白质而不会引发免疫反应阻碍其他治疗方法。
发现主要在男孩,DMD是位于性染色体的基因突变造成的,停止生产肌肉演绎的蛋白质称为肌营养不良蛋白。没有它,肌肉逐渐恶化,削弱从很小的时候开始,只有恶化。大多数病人不能走过12岁,死于心脏或呼吸衰竭时达到30多岁,尽管呼吸机帮助一些活得更长。
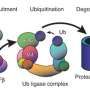
改进的基因治疗方法,多学科团队从佩雷尔曼医学院的宾夕法尼亚大学工程腺相关病毒(AAV)载体交付“替代”蛋白肌营养不良蛋白在小型和大型动物DMD模型保持肌肉完好无损。合成替代品,基于一种天然的蛋白质称为拉,被证明是一种有效和安全的选择,因为它保护肌肉与天然DMD-like突变小鼠和狗,包括一个大型删除,类似于大肌营养不良蛋白缺失发现在人类。
“第一次,我们表明的精心构建版本dystrophin-related蛋白质可以安全地防止肌肉分解并维持其功能随着时间的推移,在最有益的动物模型。这一发现对基因治疗有重要影响,我们如何工作安全有效的治疗肌肉萎缩症,”资深作者Hansell h . Stedman说,医学博士,副教授手术。“有了这些结果,我们有强烈的理由推进这个目标进入人体临床试验。”
恢复水平的抗肌萎缩蛋白基因疗法和其他技术已经在审查由于免疫系统添加它认为外国的不良反应。DMD患者几乎没有这种蛋白质,所以他们的身体可以攻击善意的直接替代蛋白质,因为他们被视为外国。然而,由于肌营养不良蛋白的远房表妹拉表示身体的其他地方,这是认为免疫系统不会把它看成是一种威胁。
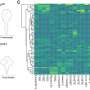
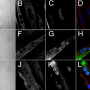
潘队显示这是真的在严谨、随机研究老鼠和狗。提供单剂治疗AAV载体的合成拉到新生鼠显示蛋白质的分布到全身,没有中毒的迹象,和完全抑制DMD的迹象,而未经处理的小鼠。拉到的老鼠也会持续表现在骨骼和心脏肌肉,和物理测试小鼠支持持续的肌肉功能。
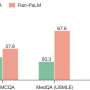
通过管理团队进一步研究拉狗4到7天的年龄在随机研究。六周后收到一剂,研究人员观察到拉到一个健壮的表达式和体重增加到了原来的4倍比之前报道的减肥和全身炎症,建议诱导免疫“汽车”狗接受人类的肌营养不良蛋白。宾夕法尼亚大学小组还观察到显著降低水平治疗肌肉损伤的狗。
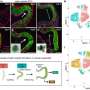
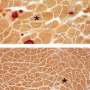
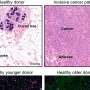
也许最重要的犬类研究中,研究人员将utrophin-treated四肢与dystrophin-treated四肢,4周后,观察到明显的不同。肌肉活检显示持久的表达拉到持续的肌肉损伤和抑制,但只有稀疏的其他肢体肌营养不良蛋白在细胞死亡。四肢之间的免疫反应也大大不同。
“在显微镜下看起来像一个手榴弹在四肢肌营养不良蛋白去了,“Stedman说。“实验表明免疫反应肌营养不良蛋白是100到1000倍拉。”
对待狗也接近完成预防肌肉变性和再生的下巴关闭(咬)肌肉。这些肌肉,由于他们的极端的权力,是第一批在治疗营养不良的狗还会恶化。
这是第一个大型动物研究显示拉的有效性以及其non-immunogenic反应。综上所述,研究人员说,这些发现可能会再次现场对使用功能优化,安全utrophin-based基因治疗方法作为潜在的治疗杜氏的路径肌肉萎缩症。
创建佩恩的合成版本,一个研究小组首先转向进化生物学,以更好地理解肌营养不良蛋白的来源以及它如何组装,回顾和重构基因事件在地球史上最早的地方。正在进行的研究将揭示更多关于蛋白质的组成,其杆结构的强度,和删除等重要特征,向未来发展。
“我们获得了很多的洞察力的方法,“Stedman说。”,我们希望做的一件事在临床开发是利用这种见解有没有更好的治疗方法,最大可能的版本的‘nanotrophin’。”
更多信息:Non-immunogenic拉到基因疗法治疗肌肉萎缩症的动物模型,自然医学(2019)。DOI: 10.1038 / s41591 - 019 - 0594 - 0,nature.com/articles/s41591 - 019 - 0594 - 0