老年痴呆症的τ蛋白远远超过在脑组织淀粉样蛋白在预测人数
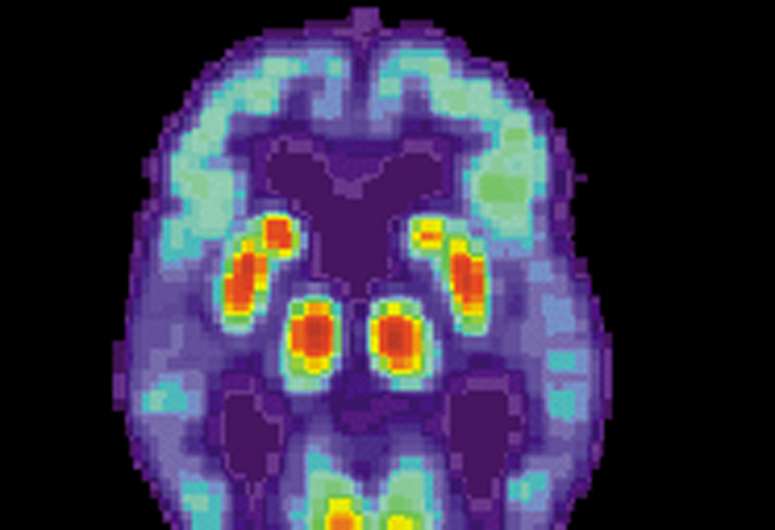
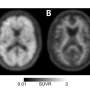
大脑成像的病理tau蛋白“缠结”可靠地预测未来脑萎缩的位置在老年痴呆症患者提前一年以上,根据一项新的研究通过旧金山加州大学的科学家们记忆和衰老中心。相比之下,淀粉样斑块,”的位置已被阿尔茨海默氏症研究和药物开发的重点几十年来,被发现的小工具在预测损失将如何展开随着疾病的进展。
结果,2020年1月1日出版科学转化医学,支持人员日益认识到τ导致阿尔茨海默病大脑退化更直接淀粉样蛋白,同时展示了最近开发的潜力tau-based PET(正电子发射断层扫描)脑成像技术来加速阿尔茨海默氏症的临床试验,提高个性化病人护理。
“τ的传播之间的匹配和大脑发生在第二年真的是惊人的,”神经学家吉尔Rabinovici说,医学博士,爱德华·费恩和珍珠Landrith特聘教授在记忆和衰老和PET成像项目领导人UCSF记忆和衰老中心。“τPET成像预测不仅我们会看到多少萎缩,但也会发生。这些预测是更强大的比我们已经能够与其他成像工具,和增加的证据表明,τ是疾病的主要因素。”
τ的兴趣增长Amyloid-Based疗法跌倒
阿尔茨海默氏症研究人员长期以来争论的相对重要性τtangles-two类型的错误折叠的蛋白质和淀粉样斑块集群在后期研究病人的大脑,阿尔茨海默在20世纪初首次发现的。几十年来,“淀粉样蛋白营”为主,导致多个高调与amyloid-targeting努力减缓阿尔茨海默氏症药物,所有令人失望或混合的结果。
许多研究人员正在一眼τ蛋白,一旦被视为一个简单“墓碑”标记细胞死亡,并调查是否τ事实上可能是一个重要的生理疾病的司机。淀粉样蛋白相比,积累广泛的大脑,有时甚至在没有症状的人,老年痴呆症患者的尸检显示,τ集中准确的脑萎缩最严重的地方,位置,有助于解释不同病人的症状(例如,在语言学习方面和与内存相关区域)。
“没有人怀疑淀粉样蛋白在阿尔茨海默氏症中扮演一个角色,但越来越多的τ发现开始转变人们思考什么是如何推动疾病,”解释Renaud乐趣,博士,博士后研究员Rabinovici体内分子神经影像实验室和新研究的主要作者。“不过,只是看着死亡的脑组织,很难证明,τ缠结导致大脑退化,而不是反过来。我们组的一个关键目标是开发非侵入性脑成像工具,让我们看看τ的位置积累在疾病的早期预测以后大脑退化。”
τPET扫描预测未来脑萎缩患者个体的位置
尽管早期的疑虑,τ可能无法测量大脑在生活,科学家最近开发出一种可注射的分子称为flortaucipir-currently正在审查由FDA-which结合错误折叠τ在大脑中,发出轻微的放射性信号可以被PET扫描。
Rabinovici和合作者威廉Jagust医学博士,加州大学伯克利分校的劳伦斯伯克利国家实验室,在第一时间采取τPET成像研究τ缠结的分布正常衰老的大脑而在一个较小的横断面研究阿尔茨海默氏症患者。他们的新研究表示第一次尝试测试τ水平在老年痴呆症患者是否可以预测未来的大脑退化。
La乐趣招募了32个参与者通过加州大学旧金山分校与阿尔茨海默病早期临床阶段记忆和衰老中心,他们收到了PET扫描使用两个不同的示踪剂测量水平τ的蛋白质和淀粉样蛋白在大脑。参与者还收到了MRI扫描测量他们大脑的结构完整性,无论是在研究开始的,在后续访问一到两年后。
研究人员发现,在参与者的大脑整体τ水平研究开始的预测多少变性将发生的时间跟进访问(平均15个月后)。此外,当地的τ累积模式预测随后的萎缩在同一位置,准确率超过40%。相比之下,基线淀粉pet扫描正确预测未来大脑退化的只有3%。
“看到τ累积预测会发生变性支持我们的假设,即τ是阿尔茨海默病的神经退化的关键驱动因素,”洛杉矶生活乐趣。
值得注意的是,PET扫描显示,年轻的参与者有更高的整体水平τ在他们的大脑,以及更强的基线τ和随后的脑萎缩之间的联系,而年长的参与者。这表明,其他因素可能会异常蛋白质或血管损伤晚发性阿尔茨海默氏症中扮演更重要的角色,研究人员说。
能够预测脑萎缩有价值的精密医学工具的
结果添加到希望tau-targeting药物目前在加州大学旧金山分校学习记忆和衰老中心和其他地方可以提供临床好处患者通过阻断关键驱动因素的神经退化疾病。同时,使用τ宠物的能力来预测后大脑退化能够更个性化的痴呆护理和速度正在进行的临床试验,作者说。
“人们想知道的第一件事当他们听到一个诊断阿尔茨海默病是什么自己或亲人的未来。它将是一个长期衰落的内存,或者快速下降到痴呆?病人能够独立生活多长时间?他们会失去说话的能力或绕过自己?目前这些问题我们无法回答,除了最一般条款,”Rabinovici说。“现在,第一次,这个工具可以让我们给患者的期望通过揭示生物过程潜在的疾病。”
Rabinovici和他的团队还预测,预测未来的能力基于τPET成像的脑萎缩将使阿尔茨海默氏症的临床试验来快速评估一个实验性的治疗是否可以改变个人的特定轨迹预测病人,目前不可能由于个体差异较大的个体与个体疾病的进展。这样的见解可以调整剂量或切换到一个不同的实验化合物如果第一个治疗并不影响τ水平或改变病人的预测轨迹的大脑萎缩。
“τ的宠物可能是极其宝贵的精密医学未来的工具临床试验”,Rabinovici说。“能够敏感地追踪τ积累生活的患者将首次让临床科研人员寻找治疗可以减缓甚至阻止的具体模式大脑萎缩预计为每一个病人。”
更多信息:Renaud La乐趣et al .前瞻性纵向萎缩在阿尔茨海默病与基线tau-PET的强度和地形,科学转化医学(2020)。DOI: 10.1126 / scitranslmed.aau5732