小说在皮肤鳞状细胞癌治疗靶点

皮肤鳞状细胞癌(cuSCC)是第二个最常见的诊断恶性肿瘤在美国,每年有大约700000新病例。累积暴露于紫外线是主要的导致cuSCC环境危险因素。虽然大多数cuSCC情况很容易管理和治疗,一小部分患者对治疗没有反应,很差的结果。莫菲特癌症中心的研究人员想要设计这类患者更好的治疗策略通过改善cuSCC如何发展他们的理解。在一个新的文章提前打印在线发表在《华尔街日报》癌症研究莫菲特科学家报告cuSCC识别潜在的治疗靶点。
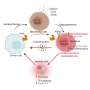
弗洛雷斯实验室都集中在识别p53突变癌症的治疗靶点。在这项研究中,团队专注于蛋白质TAp63-a的活动肿瘤抑制蛋白p53的家庭的一部分肿瘤抑制。这个家庭的蛋白质通常函数来抑制肿瘤的发展和增长。TAp63也是弥补p53损失和发挥重要作用的创作被称为小分子核糖核酸的一小段RNA存在在人类基因组中。小分子核糖核酸导致许多生物过程和经常被管制在不同的疾病,包括癌症。
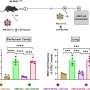
研究人员想要确定TAp63的函数作为一个肿瘤抑制和监管机构的microrna cuSCC发展的可能影响。他们失踪TAp63基因治疗小鼠和正常小鼠紫外线没有TAp63基因,发现老鼠了cuSCCs数量显著高于正常小鼠。这些观察表明,TAp63还可以作为肿瘤抑制器蛋白在皮肤上。
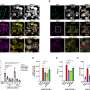
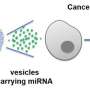
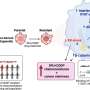
弗洛雷斯的团队然后进行了一系列比较研究在老鼠和人类cuSCC肿瘤样本,发现两个microRNAs-miR-30c-2 *和mir - 497表达在肿瘤缺乏TAp63水平要低得多。当这些小分子核糖核酸被重新引入到肿瘤细胞,发展cuSCCs明显减少。这些观察表明,miR-30c-2 *和mir - 497,类似于TAp63,可能通过抑制函数cuSCC的增长和发展。研究人员证实这个假说表明miR-30c-2 *导致细胞死亡,而mir - 497抑制细胞生长和增殖;因此,当这些microrna失踪,cuSCC可以继续无节制的增长。
该小组还进行研究,以评估下游目标的小分子核糖核酸cuSCC增长的影响。他们证明了7个基因目标的小分子核糖核酸一般管制cuSCC肿瘤,包括AURKA基因。他们证实AURKA的重要性表明抑制AURKA能够减少cuSCC增长在小鼠模型,表明AURKA可能是一个适当的治疗目标。
“我们的研究建立TAp63作为重要的抑制UV-induced cuSCC和揭示了一个之前从未描述小分子核糖核酸的功能网络和有针对性的mrna,”埃尔莎弗洛雷斯说,莫菲特博士,分子肿瘤学和癌症生物学和进化的计划。“考虑到缺乏高级cuSCC FDA批准的靶向治疗,我们的研究提供了临床前证据使用miR-30c-2 * / mir - 497交付或AURKA抑制的有效治疗方法。”
弗洛雷斯希望这将导致进一步调查这些潜在目标。
更多信息:TAp63-regulated安德鲁•约翰•戴维斯等小分子核糖核酸抑制皮肤鳞状细胞癌通过抑制细胞周期基因网络,癌症研究(2020)。DOI: 10.1158 / 0008 - 5472. - 19 - 1892