研究人员开发了进行癌症液体活检的新工具

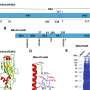
癌症是世界范围内导致死亡的主要原因之一,在转移之前的早期阶段被诊断出来,存活率要高得多。在转移过程中,循环肿瘤细胞(ctc)从原发肿瘤脱落进入血液以扩散癌症,从而引发二次生长。来自纽约大学阿布扎比分校的一个工程研究团队,由纽约大学机械和生物医学工程助理教授Mohammad A. Qasaimeh领导,开发了一种与原子力显微镜(AFM)前沿程序兼容的微流体平台。
发达平台用于从前列腺癌患者的血液样本中捕获ctc,然后在纳米尺度上对ctc进行AFM力学表征,以寻找新的转移力学生物标志物。
虽然ctc的一般生命周期在一定程度上得到了承认,但ctc在血液中循环时的寿命和相互作用仍然未知。ctc非常罕见,很难从数十亿的背景中分离出来健康的血细胞,因此它们的生物学和力学表型仍有待探索。
开发的新工具允许ctc的分离和表征,因此具有协助癌症早期检测的潜力。它还可以作为一种工具,更有效地跟踪和监测癌症进展和转移。
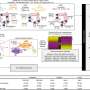
论文题为afm兼容的微流体平台,用于基于亲和力的循环肿瘤细胞的捕获和纳米力学表征微系统与纳米工程杂志上,研究人员介绍了他们开发的微流控技术,从血液样本中分离ctc,以进行进一步分析。ctc是从其他血液中分离出来的细胞通过观察它们对不同单克隆抗体亲和力的差异。开发的工具是一个组合的微流体-AFM平台,其中AFM分析可以用于研究捕获的ctc癌细胞的弹性和粘附性能。

ctc是癌症检测、诊断和预后的生物标志物。随着ctc在血液中扩散,利用其发现的特征,可以通过液体活检程序将其去除。分离的ctc可以潜在地用于药物测试和精确癌症治疗的分子分析。液体活检的侵入性远小于传统的组织活检,在不久的将来有可能取代传统的组织活检,并在当地的诊所或药房进行。
Mohammad a . Qasaimeh说:“我们预计,通过在单细胞水平上识别CTCs的机械和生物表型,这个平台可能成为癌症诊断和预后的潜在非常强大的工具。”
“通过轻微的定制,该平台也可以适用于包括乳腺癌和肺癌在内的其他类型的癌症,”该研究的第一作者、纽约大学工程研究科学家穆罕默德·德勒曼(Muhammedin Deliorman)说。
作者希望使用开发的工具,捕获的ctc的纳米力学特性可以在未来帮助识别侵袭性癌症用于开发更有效的治疗方法。
进一步探索