淋巴瘤的不同路径显示
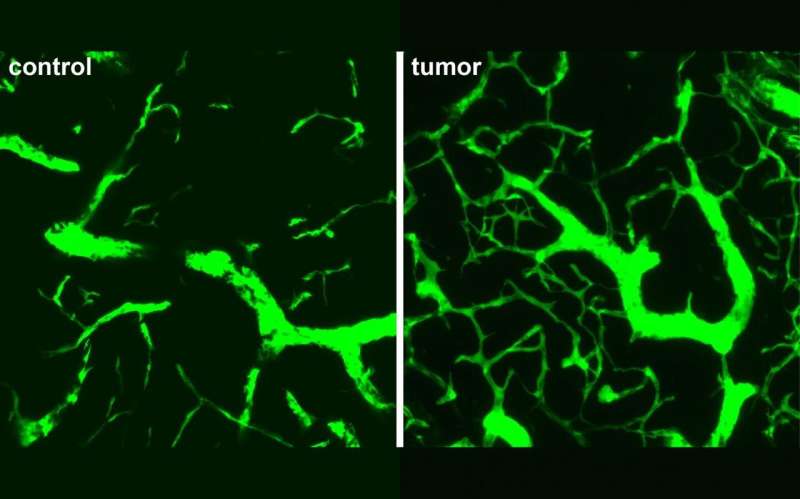
Helmholtz协会(MDC)的Max Delbrueck分子医学中心的一个团队在该杂志上报告说,淋巴结肿瘤的血管生成过程不同于结肠或肺等身体其他部位的肿瘤癌症研究。MDC实验室的科学家阿明·雷姆博士、乌塔博士Höpken和霍尔格·格哈特教授都参与了这个项目。该团队确定了可能更有效的治疗靶点,以减缓淋巴瘤患者的肿瘤生长。
淋巴瘤是淋巴系统的癌症,包括淋巴结,脾脏和骨髓。有血管发展增加指标的淋巴瘤患者通常有较低的生存机会。它们对已经成功抑制其他类型癌症血管发展的治疗效果也不好。
“我们假设淋巴结肿瘤与实体肿瘤完全不同,因为淋巴结为血液传播提供了如此有利的微环境肿瘤细胞Uta博士Höpken说,他领导MDC的自身免疫和癌症实验室的微环境调控。然而,MDC转化肿瘤免疫学实验室的负责人阿明·雷姆博士说,“绝对令人惊讶的是,没有一个通常的嫌疑人参与其中。”
消除怀疑
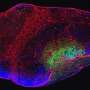
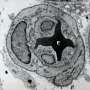
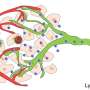
早期淋巴瘤的血管异常致密和不规则,与健康淋巴结的血管相比有更多的分支。在中未观察到分枝的模式实体肿瘤在受感染的淋巴结或正在发育的器官中,这些部位通常是新血管生成的其他部位。
为了揭示驱动这一发展的独特信号通路,研究小组使用发生淋巴瘤的转基因小鼠模型和被植入淋巴瘤的小鼠模型进行了分析细胞。他们看了看基因表达模式观察哪些基因和蛋白质在肿瘤发展的初始阶段最活跃。
通常与肿瘤血管生成有关的罪魁祸首——炎症,低氧水平而血管基部和血管尖端之间的信号,即Notch信号,在研究结果中没有显示出来。
成功的街区
一组被称为血管内皮生长因子(VEGF)的蛋白质被认为是正常的主要驱动因素血管的发展,以及肿瘤中的血管生成。在大多数实体瘤中,VEGF-A是介导这一过程的蛋白质,与它的受体VEGFR-2一起。
在淋巴瘤的早期阶段,研究小组发现VEGF-C是最活跃的蛋白质。当他们试图阻止受体VEGFR-2来抑制VEGF-C活性时,没有任何改变。
但当研究人员阻断了另一种受体VEGFR-3时,血血管生长明显减慢。他们还中断了一种叫做淋巴毒素的小蛋白质的受体,这种蛋白质通常是正常淋巴结发育所必需的,它也有助于减缓血管生成。
该团队使用了两种已经被批准的药物临床使用抑制自身免疫性疾病的途径。他们证实这种治疗也有效人类细胞。虽然不是临床医生自己,但研究人员希望这种疗法可以用于临床试验,以调查其在人类患者中的有效性。Rehm说:“如果少数癌细胞能通过化疗存活下来,就有可能通过免疫疗法解决这些途径来预防复发。”
从一开始就观察
这项研究的一个关键特征是时间。研究人员在癌细胞侵袭淋巴结后的前12天内追踪血管生成。这给了他们一个独特的机会,可以观察肿瘤细胞和淋巴结微环境之间的早期“串扰”或相互作用。只有五到10%的淋巴结细胞癌是癌变,并且已经重组了淋巴结。“我们看到的变化很早,肿瘤负担很低,”Höpken说。
成像这些早期的高分辨率变化提出了一个需要大量勤奋的挑战。“淋巴瘤细胞是高度分区的淋巴结内的广泛分布细胞,”翻译肿瘤潜水员局部实验室中的Lutz Menzel,Co-First Author和Post Doc说。“发现淋巴瘤引起的基质的重塑,当淋巴结的其他区域仍未受到影响时,通常经常在显微镜下寻找”干草堆“中的”针“。”
该团队强调了动物在这项工作中的重要性。这样的研究在人类病人身上是不可能的,因为他们还没有表现出症状。Rehm说:“动物提供的优势是在疾病开始时看到发生了什么,而不是在疾病结束时。”“要模拟复杂淋巴结组织中多种不同细胞类型之间的相互作用,类器官还远远不够。”
该小组计划继续调查两者之间的关系肿瘤细胞和淋巴结微环境,看看单细胞测序是否能揭示更多关于血管生成过程的信息。
进一步探索





用户评论