机械工程师开发肿瘤模型,更敏感地模仿身体

研究界越来越升高,肿瘤环境的生物力学可能导致其细胞如何生长,甚至在整个身体上蔓延的方式。更接近的研究人员可以重新创造实验室中的那些机械因素,越好,他们将理解肿瘤细胞迁移以及如何在侵入其他组织之前停止细胞。
在最近发表的研究中Acta Biomaterialia.一支瑞森勒工业研究所的机械工程师团队展示了一种新的技术,用于在体外创造一个用于研究更复杂的肿瘤的生物模型,因此更接近什么癌细胞可能会在身体中遇到。
“我们越来越靠近胶原蛋白在组织中组织的架构,而不是迄今为止的任何其他基于胶原蛋白的模型,”机械,航空航天助理教授克里斯汀厂说核工程在Rensselaer,以及生物技术和跨学科研究中心的成员。
胶原是构成细胞外部结构的主要蛋白质,称为细胞外基质。因此,它通常也是用于生长的体外模型的主要成分肿瘤细胞在实验室里。
基于胶原的细胞外矩阵模型的刚度问题是因为,因为磨坊已经看到以前的研究,僵硬的变化给出了瘤一种有助于的结构提示癌症进展。创建可以模拟可调谐刚度的模型很重要。
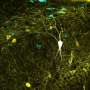
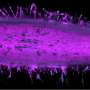
研究人员还发现,在体内 - 在生物体内 - 胶原细胞外基质的结构在癌症进展中起着作用。在肿瘤环境中,胶原蛋白形成纤维束,以作为分类的高速公路,癌症细胞迁移出肿瘤以侵入其他组织。在形成过程中,米尔斯表示,这些纤维束采用特定的尺寸和结构,被认为让细胞更容易地传播。现在,该过程尚未完全清楚,这使得创建模型,模拟这种结构更加密切。
“我们注意到那些纤维结构通常比实验室中创造的那些大得多,因此这是为了创造更好的肿瘤相关模型细胞外基质,“Xiangyu Gong说,他最近赢得了他的博士学位。在Renselaer的Mills Lab的机械工程中,现在是耶鲁大学的博士后研究员。
Rensselaer团队能够找到离子强度和温度的正确组合,以诱导胶原蛋白 - 已经从组织中分离 - 形成微米级束而不是通常用于癌症研究的纳米级纤维凝胶。然后,研究人员创造了一种微流体通道,以使捆绑的束缚 - 就像它们在体内一样。
“我们现在可以研究癌细胞如何与胶原束相互作用,其中有一些在体内可以看出的大小规模,”米尔斯说。“现在可以研究这个过程,迁移。”
“我们发现这些侵略性癌细胞将遵循我们创建的这些高速公路,看起来与试图离开原始肿瘤部位的这些癌细胞的体内图像非常相似,”龚说。
这种新方法允许研究人员将新创建的胶原捆与一种凝胶类型的凝胶相结合,其刚度可以调整,以便提供更准确和可控的凝胶模型这可以模仿身体内的组织的结构和与肿瘤连通的机械线索。
Mills和Gong希望这项研究提供了更广泛的信息,了解使用复杂和整体模型更加密切地模仿体系肿瘤细胞在体内遇到的肿瘤细胞。
进一步探索











用户评论