利用糖分会让肿瘤细胞的信号通路中断某种特定的药物的影响
LMU科学家们表明,一个中断的信号通路在尤因肉瘤特别是糖分会让肿瘤细胞特定的药物。这一发现可能会打开一个路线最激进的形式的疾病的新疗法。
尤因肉瘤是第二个最常见的类型的骨癌在儿童和青少年中找到。自发突变,导致致癌基因融合的形成,是这种疾病的发病的先决条件。被融合癌基因激活其他基因编码的蛋白质,并触发这一过程可以进展到恶性阶段。疾病的相对严重程度可能受到出席其他基因位点的遗传变异的本质在单独的融合致癌基因的载体。LMU领导的研究人员托马斯•Grunewald Max-Eder研究小组的领导人LMU儿科肉瘤生物学研究所的病理学和德国癌症研究中心的一个部门主管(DKFZ)海德堡已经确定了一个基因的异常激活的融合致癌因素表明,它使肿瘤选择性容易药理攻击。这个项目主要是由德国癌症援助(德意志Krebshilfe),和发现发表在在线杂志自然通讯。
尤因肉瘤的治疗可用的治疗策略是有限的,这一事实证明了在大约三分之一的病人,肿瘤缓解最终之后常常fatal-relapse。这凸显了需要进行替代治疗恶性肿瘤的方法。”由于种种原因,被融合致癌基因编码的蛋白质本身并不是一个合适的药物目标,“Grunewald说。”,所以我们开始寻找替代目标之间的融合基因被激活的癌基因,专注于那些已知参与控制骨骼的正常发展。这个搜索显示,基因SOX6明显在尤因肉瘤”。During the normal growth of bone, SOX6 is activated for a short time only, and triggers a massive but brief burst of cell proliferation. "When we silenced the activity of SOX6 in细胞系来自尤因肉瘤患者的细胞和肿瘤生长速度显著降低我们的模型系统。我们假设SOX6融合不断激活的癌基因,而这部分占这些肿瘤的无节制的增长,“Grunewald说。
事实上,SOX6信号通路管制在尤因肉瘤细胞原则上应该使他们特别容易消除,因为SOX6也诱发细胞应激反应的蛋白质。
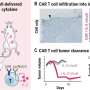
因此,细胞中的蛋白过表达应该产生较高的活性氧(ROS)比其他细胞。这个功能应该反过来做肿瘤细胞对Elesclomol特别敏感。最初开发用于治疗恶性黑素瘤,这种化合物同样促进活性氧的生成。“由于细胞过表达SOX6已经包含大量的活性氧,接触Elesclomol应该提高浓度超出诱导细胞死亡所需的水平,”Grunewald解释道。“此外,这种效应可能相对肿瘤细胞的选择性,因为细胞与正常水平的SOX6不太可能达到ROS的临界浓度即使在Elesclomol的存在。”Indeed,实验室研究在传统的细胞培养和三维骨骼模型证实Elesclomol显著减少尤因肉瘤细胞具有较高的可行性SOX6活动相对于那些SOX6合成少量的蛋白质。实验小鼠模型还显示,Elesclomol减少肿瘤的生长。
基于这些结果,Grunewald和他的同事们相信Elesclomol代表一个有前途的治疗选择尤因肉瘤患者的肿瘤表现出强烈的SOX6超表达。“SOX6表达水平不同病人的病人。发现高水平尤其是在病人携带特定基因变异放大的主要的影响融合基因和加速扩散肿瘤细胞,”他说。“到目前为止,这些患者可能有比其他人更糟糕情况。”