在ALS恢复肌肉紧张沟通
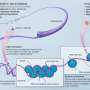
患者肌萎缩性脊髓侧索硬化症(ALS),也被称为卢伽雷氏症,失去肌肉控制大脑和脊髓神经细胞或神经元退化,可以不再发送信号的肌肉。突触,先前的研究已经发现问题的信号从一个神经元跳到另一个神经元或肌肉,可以导致断开连接。但目前还不清楚是什么原因导致这些问题。杰斐逊温伯格ALS中心的新的研究发现了一种机制,通过这种机制的形成有毒proteins-a ALS-disrupts神经传输的共同特点。这些发现提供了一个为了解如何保持肌肉紧张连接在肌萎缩性侧索硬化症,,有可能导致寻找新疗法。该研究发表在EMBO分子医学2020年4月29日。
继承例ALS背后的罪魁祸首是经常C9orf72基因的一个错误,错误的指示细胞,企业重复序列的蛋白质,称为二肽重复序列(dpr)。最丰富的dpr之一是GA蛋白质,形成聚集,逐渐引起毒性可以杀死神经元。
“我们的合作者在德国找到了在前一个小鼠模型GA超量产生有赤字运动机能大卫。Trotti,解释说:“博士,神经科学教授研究温伯格ALS中心的主任和文章的第二作者的研究。“但我们不知道GA在神经元本身。”
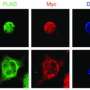
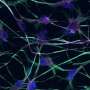
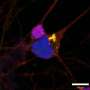
研究人员培养运动神经元,神经元连接到肌肉,从老鼠到仔细看看GA总量。他们发现GA总量实际上是移动、旅行在神经元和积累树突和轴突,突触被发现的地方。研究人员还发现,GA骨料的存在导致钙离子的大量涌入,破坏神经元的电平衡。这种不平衡可能损害神经元的能力检测和发送信号。
实际上,当研究人员检测了神经元的突触机械负责发送信号到肌肉,他们发现关键蛋白的减少突触囊泡在运动神经元生长相关蛋白2 (SV2)或在培养皿中培养。SV2调节释放神经递质,是神经元的信号分子相互通信和肌肉。
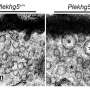
这SV2下降导致减少释放神经递质,防止神经元正常沟通与肌肉。重要的是,这种减少SV2还发现体内GA neuron-muscle连接在一个小鼠模型的聚合,以及马达神经元来自诱导多能干细胞(万能)C9orf72形式的ALS患者。
“结果表明,这些障碍在神经传播也发生在患者的细胞,”说Piera Pasinelli,博士,神经科学教授,温伯格ALS中心的主任和文章的第二作者的研究。
“这有助于我们理解最终观察患者症状的基础。重要的是,它帮助识别目标和机制在GA disease-relevant系统不是人为地制造或过度。”
利用基因工具,然后研究人员补充SV2蛋白培养运动神经元GA聚合,发现突触功能恢复到正常水平。恢复SV2也减少毒性通常由GA聚集,甚至阻止细胞死亡和长期生存。值得注意的是,赤字SV2和突触传递发生在毒性和细胞死亡之前,所以干预时间窗可以大大有利于减缓疾病进展。
“我们已经表明,即使GA总量仍然存在,补充SV2蛋白可以战斗最不利影响蛋白质的堆积,”布里吉特·詹森说,博士,博士后温伯格中心和这项研究的第一作者。“这指向SV2作为一个有前途的治疗目标,这种遗传形式的肌萎缩性侧索硬化症。”
“我们现在有一个更好地了解是什么导致肌肉紧张的退化连接在这个毁灭性的疾病”Pasinelli博士说。
“未来的研究将有助于确定SV2可延长肌肉力量和缓慢疾病进展在C9orf72-ALS病人,”Trotti博士补充说。
更多信息:布里吉特K Jensen et al,突触功能障碍引起的甘氨酸检测丙氨酸二肽进入C9orf72 ALS / SV 2补充FTD获救了,EMBO分子医学(2020)。DOI: 10.15252 / emmm.201910722