新型冠状病毒小鼠模型将加速药物、疫苗的研究

全球快速开发COVID-19药物和疫苗的努力受到了数量有限的实验室小鼠的阻碍,这些实验室小鼠容易感染导致COVID-19的SARS-CoV-2病毒。现在,圣路易斯华盛顿大学医学院的研究人员报告说,他们已经开发出一种COVID-19小鼠模型,可以在人身上复制这种疾病。此外,其他科学家可以很容易地采用同样的方法,大幅加快对实验性COVID-19治疗和预防措施的测试。
的小鼠模型在6月10日在线发表的一篇论文中描述了细胞。除了药物和疫苗测试外,科学家还可以将该模型用于老鼠为了发展而培育健康状况如肥胖,糖尿病或慢性肺病调查为什么一些人患上了危及生命的COVID-19病例,而另一些人则自行康复。
首席研究员迈克尔·s·戴蒙德医学博士、赫伯特·s·加瑟医学教授和病毒感染专家说:“人们迫切希望尽快开发疫苗和治疗方法,由于动物模型有限,这些试验性药物和疫苗已经直接用于人体,其中许多都没有成功。”“老鼠是有用的,因为你可以研究大量的老鼠,观察疾病和疾病的过程免疫反应这在人身上很难做到。如果我们能获得更多关于这些潜在药物和疫苗如何工作的信息,以及它们的效果如何,那么在我们转向更具挑战性的非人类灵长类动物之前,对人们来说,这将更划算,更有效,更安全人类研究."
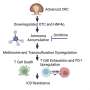
老鼠不会自然感染病毒导致COVID-19。为了感染人类,这种病毒会附着在呼吸道细胞表面的一种叫做血管紧张素转换酶-2 (ACE2)的蛋白质上。但是人类的ACE2蛋白与小鼠的ACE2蛋白不同,病毒无法附着在小鼠的ACE2蛋白上。
导致2003年SARS流行的病毒与导致COVID-19流行的病毒密切相关,SARS病毒也通过附着在人类ACE2蛋白上感染细胞。在SARS流行期间,研究人员培育了一种含有人类ACE2蛋白的转基因小鼠,以便研究SARS。然而,在疫情结束后,人们对SARS的兴趣减弱了,老鼠的聚居地也关闭了。今年早些时候新冠病毒的出现引发了人们疯狂地重新开始培育小鼠,但即使是现在,也没有足够的小鼠供所有想要研究这种疾病、测试潜在疫苗和治疗方法的研究人员使用。
戴蒙德此前曾领导开发了寨卡病毒感染小鼠模型,他意识到他们需要一种更快的方法来获得可用于COVID-19研究的小鼠。Diamond和他的同事们——包括共同第一作者Ahmed Hassan, DVM博士,和Brett Case博士,都是博士后研究员,以及Emma Winkler,医学博士/博士。戴蒙德实验室的一名研究生以及其他几名COVID-19团队的主要成员决定暂时将人类ACE2蛋白引入小鼠体内。为了做到这一点,他们将人类ACE2基因插入一种被称为腺病毒的温和呼吸道病毒中。他们还去除了腺病毒复制所需的基因,这样病毒就可以感染细胞一次,但不能繁殖。然后,研究人员用改良的腺病毒感染小鼠。这些动物的呼吸道中产生了人类ACE2几天,使它们很容易感染导致COVID-19的病毒。
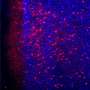
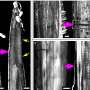
为了观察小鼠是否会患上与人类类似的疾病,研究人员用改良的腺病毒感染了小鼠,五天后通过鼻子给它们注射了COVID-19病毒。这种病毒迅速地沿着海岸传播呼吸道尤其是对肺部,它在肺部大量复制,并引起肺炎和明显的炎症,就像在人类身上一样。研究人员还发现,心脏、脾脏和大脑中的病毒水平较低——这些器官都可能成为人类病毒的目标。这些老鼠在患病期间体重下降了10%到25%,但最终恢复了健康。
身为分子微生物学、病理学和免疫学教授的戴蒙德说:“老鼠患上了与我们在人类身上看到的相似的肺部疾病。”“他们会病一段时间,但最终会康复,就像绝大多数感染COVID-19的人一样。你可以对几乎任何一种实验室小鼠使用这种技术,使它们对SARS-CoV-2敏感,然后做任何你想做的研究:测试疫苗或药物,研究免疫反应,以及与病毒如何致病有关的许多其他事情。”
该模型还可用于更好地了解使一些人面临严重COVID-19疾病风险的因素。高龄、男性以及肥胖、糖尿病、心脏、肾脏或肺部疾病等都会增加患严重COVID-19的风险,其原因尚不完全清楚。
戴蒙德说:“例如,研究老年小鼠或肥胖小鼠并观察它们对感染的反应是很容易的。”“我预计他们会做得更糟,但真正的问题是为什么。他们在早期是否有更多的病毒?他们的状况是否削弱了免疫反应,或者可能加剧了有害的炎症反应?有了这个模型,我们可以开始研究那些很难在人类身上研究的因素。”