δ阿片受体识别为有前途的治疗炎性疼痛缓解的目标

δ阿片受体有内置机制来缓解疼痛,可以精确靶向药物传输nanoparticles-making他们的承诺目标治疗慢性炎性疼痛用更少的副作用,根据一项新的研究中一个国际研究小组的研究人员。该研究发表在美国国家科学院院刊》(PNAS),进行了利用人类和老鼠的细胞与炎性肠道疾病,可导致慢性疼痛。
阿片样物质受体——主要是位于整个中枢神经系统和阿片类药物gut-relieve疼痛时被激活,这两个自然产生的身体和那些作为药物。虽然有几种类型的阿片受体,大多数羟考酮和吗啡等阿片类药物作用于μ阿片受体。阿片类药物有显著的副作用的μ阿片受体,包括便秘和呼吸困难。这些药物成瘾及其有效性随时间减少,所以人们需要高剂量来管理他们的痛苦,导致增加的副作用和过量的风险。
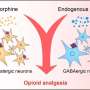
在这项研究中,研究人员专注于不同的阿片类受体:δ阿片受体,抑制疼痛时激活,但提供了一个有前途的目标治疗疼痛用更少的副作用。使用冒号的活检人和小鼠溃疡性结肠炎,炎症性肠病,研究人员发现,δ阿片受体提供了一个内置的机制来缓解炎性疼痛。的炎症细胞从结肠释放自己的阿片类药物,激活δ阿片受体,阻止肠道神经元的活动,传递疼痛信号。
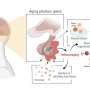
重要的是,研究人员还发现δ阿片受体细胞内的信号从一个舱称为endosome-not就在细胞表面的,正如前面的想法。在核内体,受体信号在很长时期内,这意味着δ阿片受体可以抑制疼痛更长的时间。这种持续减少兴奋性(测量疼痛)被发现当δ阿片受体被激活的炎症细胞的研究。
“我们已经表明,δ阿片受体有一个内在的机制的疼痛控制和抑制疼痛信号在一个核内体。有了这个新知识,我们认为受体是一种很有前途的治疗目标慢性炎性疼痛奈杰尔•Bunnett资深作者说:“博士,教授和系主任的分子病理学在纽约大学牙科学院(纽约)。
针对δ阿片受体,研究人员封装一个叫做DADLE止痛药,δ阿片受体结合,内部nanoparticles-microscopic车辆用于运载药物细胞。然后涂纳米粒子与相同的止痛药,专门将纳米粒子的控制疼痛和神经细胞与其他细胞类型,避免副作用。
“把药物纳入到纳米颗粒可以提高药物的稳定性和交付,提高他们的效率和经常需要小剂量和小,更有针对性的剂量降低药物的风险造成的副作用,”Bunnett说。
与神经细胞的受体结合后,纳米颗粒进入细胞达到核内体,然后慢慢地释放了止痛药来激活δ阿片受体。这导致一个长期的δ阿片受体的激活,建议持续抑制炎性疼痛的能力。
“我们的发现证明,不仅是三角洲阿片样物质受体在核内体一个内置的疼痛控制的机制,也是一个可行的治疗目标,减轻慢性炎性疼痛,“Bunnett说。
Bunnett此前进行的研究和他的同事使用纳米粒子提供阻止了不同类型的受体的药物来缓解疼痛,虽然PNAS研究集中在提供药物激活δ阿片受体。研究人员假设有效的疼痛控制将涉及阻塞和激活多个pain-transmitting通路同时,这可能会导致封装药物纳米颗粒内部的组合。












用户评论