发现参与自身免疫性眼病的分子的双重作用
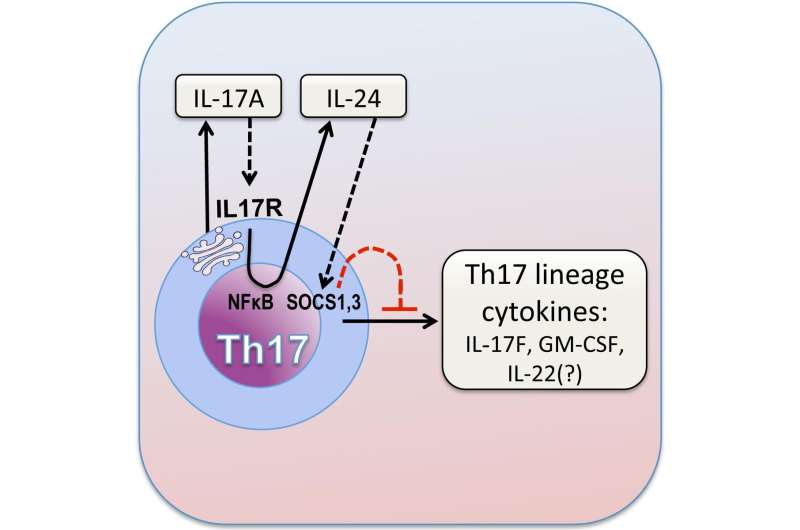
根据美国国家眼科研究所(NEI)研究人员的一项研究,炎症分子白细胞介素- 17a (IL-17A)触发免疫细胞,从而降低IL-17A的促炎活性。在眼和脑自身免疫性疾病的模型中,阻断IL-17A会增加Th17细胞产生的其他炎症分子的存在,Th17细胞是产生IL-17A并参与神经炎症的免疫细胞。这一发现可以解释为什么针对眼病自身免疫性葡萄膜炎和多发性硬化症(MS)等疾病的il -17靶向治疗失败。有关研究结果的报告发表在免疫力.NEI是美国国立卫生研究院的一部分。
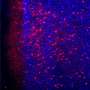
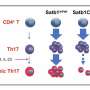
自身免疫性葡萄膜炎是免疫的细胞变得异常激活并开始破坏健康的细胞,包括光感受器和神经元。参与这种反应的关键免疫细胞是Th17淋巴细胞,它产生几种促炎分子,称为细胞因子。Th17细胞的一个特征是能够产生IL-17A,而IL-17A具有吸引力免疫细胞叫做中性粒细胞,会破坏组织。然而,多项阻断IL-17A的药物临床试验未能帮助自身免疫性葡萄膜炎或MS患者。
NEI免疫学实验室主任、该研究的资深作者Rachel Caspi博士说:“IL-17是神经-视网膜和大脑中自身免疫的典型炎症免疫分子,但它所起的作用存在一些争议。”“在我们的自身免疫性葡萄膜炎模型中,我们注意到,没有IL-17,组织损伤的数量意外地保持不变,其他炎症分子的水平更高。”
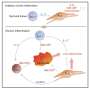
Caspi和同事使用小鼠模型来研究IL-17A在疾病过程中的作用。研究人员能够选择性地从Th17细胞中去除IL-17A,并在葡萄膜炎和ms模型中检测细胞的行为,令人好奇的是,他们发现这些细胞产生更多的IL-17F、GM-CSF和可能的其他炎症分子.研究人员得出结论,这些额外的炎症细胞因子弥补了IL-17A在驱动炎症中的损失。
卡斯皮说:“我们问自己,这是怎么回事。”“科学家就像小孩子,当他们得到一个问题的答案时,马上就会有下一个层次的‘为什么’。所以我们开始研究使整个事情起作用的更深层次的机制。”
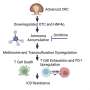
通常,IL-17A信号被其他携带IL-17受体的细胞(包括视网膜组织细胞和中性粒细胞)接收。这种受体是一种细胞表面蛋白细胞,它与IL-17A像锁和钥匙一样匹配。但在这种情况下,研究人员在最初制造IL-17A的Th17细胞表面发现了IL-17受体的副本。
“细胞结合它们自己产生的信号的过程——称为自分泌信号——已知偶尔会发生在其他类型的细胞中。但之前从未在Th17细胞中发现过。”
Caspi和同事发现,当IL-17A与Th17细胞上的受体结合时,会触发一个信号级联,从而增加细胞产生一种抗炎分子,白细胞介素-24 (IL-24),这是以前不知道由Th17细胞产生的。IL-24反过来抑制其余的Th17细胞的炎症程序,降低细胞因子如IL-17F、GM-CSF和可能的IL-22的产生。因此,如果没有IL-17A,这种自分泌循环就不会发生,从而导致Th17细胞过度产生其他炎症细胞因子,从而增加炎症。
IL-17A与几种葡萄膜炎有关,这种疾病导致美国高达15%的失明病例,葡萄膜炎通常用类固醇治疗,这可能有严重的副作用。
“有一些疾病,如牛皮癣,抗il - 17a疗法已经非常成功。我们预计这也适用于葡萄膜炎,但事实并非如此,”卡斯皮说。“这项研究可能解释了为什么针对IL-17A治疗葡萄膜炎的临床试验不成功,并表明涉及IL-17A和IL-24的联合方法可能更有效地治疗神经系统自身免疫性疾病。”