研究人员为SARS-COV-2开发了新的鼠标模型
耶鲁大学医学院的研究人员开发了一种新的小鼠模型,以研究SARS-COV-2感染和疾病,并加速对新型冠状病毒的新型治疗和疫苗的测试。该研究今天发表在实验医学杂志(JEM)还表明,关键的抗病毒信号蛋白实际上可能导致与Covid-19相关的大部分组织损伤,而不是保护肺部,而不是保护肺部。
迫切需要估算SARS-COV-2感染和疾病的动物模型,以帮助研究人员了解病毒,开发疗法并确定潜在的疫苗候选者。小鼠是最广泛使用的实验室动物,但不能感染SARS-COV-2,因为该病毒无法使用ACE2的小鼠版本,ACE2是该病毒进入的细胞表面受体蛋白人类细胞。
SARS-COV-2可以感染经过基因工程的小鼠,以产生ACE2的人类版本。然而,这些动物的可用性很低,仅限于单一小鼠菌株,从而阻止了研究人员研究病毒如何影响免疫功能低下或肥胖的小鼠,从而大大增加了人类死亡率。
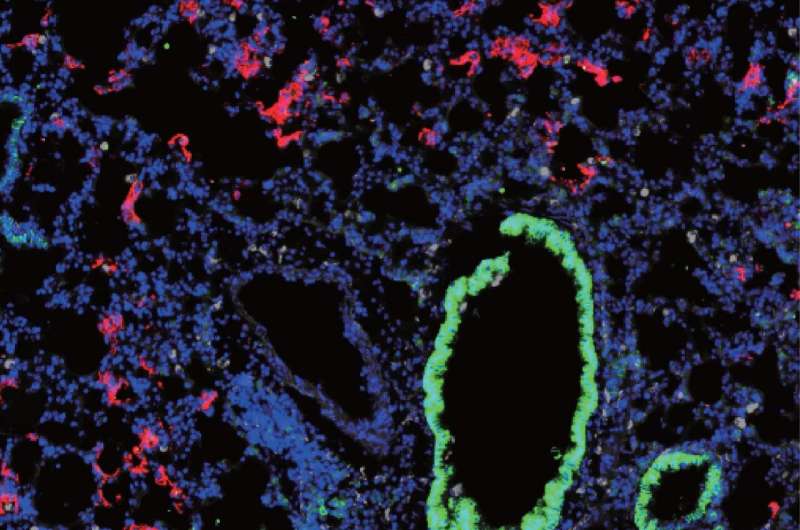
在新研究中,由耶鲁大学医学院Akiko Iwasaki领导的一组研究人员开发了一种SARS-COV-2感染的小鼠模型,其中动物首先感染了携带人ACE2基因的不同,无害的病毒。感染该病毒的小鼠会产生人ACE2蛋白,然后被SARS-COV-2感染。Iwasaki及其同事发现SARS-COV-2可以在这些小鼠中复制并诱导炎症反应类似于在Covid-19患者中观察到的,在这种情况下,各种免疫细胞被激活并募集到肺部。伊瓦萨基说:“此外,感染的小鼠还迅速发展了针对SARS-COV-2的中和抗体。”
人体对病毒感染的反应通常取决于称为I型干扰素的信号分子,该分子可以激活免疫细胞并诱导抗病毒蛋白和抗体的产生。但是,过多的I类干扰素,尤其是在延迟产量时会导致过度的炎症和组织损伤。实际上,尽管I型干扰素信号传导可预防相关的冠状病毒MERS-COV,但它会响应SARS-COV-1造成肺损伤,SARS-COV-1是导致2002 - 2003年以前的冠状病毒爆发的病毒。
目前尚不清楚I型干扰素在Covid-19中的作用。伊瓦萨基(Iwasaki)及其同事发现,类似于19例Covid-19患者,感染了SARS-COV-2的小鼠会激活与I型干扰素信号传导相关的大量基因。然后,研究人员使用其模型系统感染缺乏I型关键组成部分的小鼠干扰素途径,发现它们在控制SARS-COV-2感染方面并没有更糟。但是,这些动物招募了较少的炎性免疫细胞进入其肺部。Iwasaki说:“这些结果表明,I型干扰素不限制SARS-COV-2复制,但它们可能在COVID-19呼吸道炎症中起病理作用。”“这尤其令人担忧,因为I型干扰素目前正在用作Covid-19的治疗方法。IFN治疗的早期时机对于提供保护和利益至关重要。”
伊瓦萨基补充说:“鼠标模型我们开发了广泛可用且高度适应的动物模型了解SARS-COV-2病毒感染,复制,发病机理的关键方面,并使用真实的患者衍生病毒。该模型提供了一个至关重要的平台,用于测试对抗Covid-19的预防性和治疗策略。”










用户评论