在开始之前停止蛀牙 - 没有杀死细菌

口服细菌可以在牙科卫生员完成牙齿上刮下牙菌斑的那一刻就可以采取行动。食用糖或其他碳水化合物会导致细菌迅速重建这种坚硬而粘稠的生物膜,并产生腐蚀牙齿搪瓷的酸,从而导致空腔。科学家现在报告了一种治疗方法,有一天可以使用一种新型的葡萄纳米颗粒配方,该治疗方法首先形成,并在牙医办公室使用新型葡萄纳米颗粒配方。
研究人员将在2020年秋季虚拟会议和博览会上今天在美国化学学会(ACS)上朝着这一目标迈进。
嘴里有700多个细菌该项目的主要研究员Russell Pesavento博士说。它们包括有益细菌这有助于消化食物或检查其他微生物。它们还包括有害链球菌物种,包括链球菌突变。清洁后不久,这些细菌粘在牙齿上并开始繁殖。以糖为能源和构建块,微生物逐渐形成了一部坚韧的薄膜,无法通过刷牙轻松去除。随着细菌继续代谢糖,它们产生酸副产物溶解牙釉质,为空腔铺平道路。
牙医和消费者可以与包括氟化物在内的产品进行反击,以抑制斑块和硝酸银或二硫胺氟化物以阻止现有的蛀牙。研究人员还研究了由氧化锌,氧化铜或银以治疗牙齿感染。伊利诺伊州芝加哥大学伊利诺伊大学的佩萨文托(Pesavento)表示,尽管诸如此类的杀菌剂在牙科中占有一席之地,但重复的应用可能会导致牙齿染色和细菌耐药性。他解释说:“此外,这些代理人不是选择性的,因此它们在您的口腔中杀死了许多类型的细菌,甚至是好细菌。”
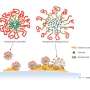
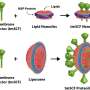
因此,Pesavento希望找到一种不会毫不差一点杀死细菌的替代方法,这将有助于防止蛀牙,而不是在事后治疗蛀牙。他和他的研究小组转向氧化葡萄纳米颗粒。其他团队研究了各种类型的氧化葡萄纳米颗粒对微生物的影响,尽管只有少数人研究了它们对初始生物膜形成条件下的临床相关细菌的影响。那些这样做通过氧化还原反应或pH驱动的降水反应或从商业来源购买纳米颗粒的人。那些先前的配方也没有作用,甚至促进了生物膜的生长实验室测试, 他说。
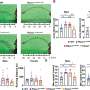
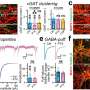
但是佩萨文托坚持不懈,因为纳米颗粒的特性和行为至少部分取决于它们的准备方式。他的团队通过将硝酸铵或硫酸盐盐溶解在水中来生产纳米颗粒。其他研究人员以前曾以这种方式制作颗粒,但没有测试其对生物膜的影响。当研究人员将聚苯乙烯板播种时S. Mutans在生长培养基中,在存在氧化葡萄纳米颗粒溶液的情况下喂食细菌糖,他们发现与没有纳米颗粒的板相比,该配方使生物膜生长降低了40%,尽管它们无法驱逐现有的生物膜。在类似的条件下,硝酸银(牙医使用的已知抗腔剂)表明对生物膜生长。
“我们治疗的优点是,它看起来不太有害口服细菌,在许多情况下,在许多情况下都没有杀死它们。硝酸银。
佩萨万托(Pesavento)在7月获得专利,他想将纳米颗粒与搪瓷强度加长的氟化物相结合,以牙医可以在患者的牙齿上绘画。但是,他指出,在实现这一概念之前,必须做很多工作。目前,团队正在尝试涂料以稳定纳米颗粒在中性或略微碱性的pH下,唾液的pH值比目前的酸性溶液更健康。他的团队还开始使用与牙龈炎发展有关的细菌,并发现一种特定的涂层纳米颗粒,该纳米颗粒量限制了在类似条件下限制依从物生物膜的形成。Pesavento和他的团队将在通常存在于口腔中存在的其他细菌菌株的情况下继续测试治疗,并测试其对下消化道人类细胞的影响,以更好地对患者有更好的整体安全感。
进一步探索
抽象的
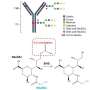
长期以来,链球菌突变一直是口腔医学领域抗菌治疗的目标。S. mutans产生强大的牙齿传播生物膜,在龋齿和牙源性感染的进展中起关键的病因学因素。基于银的杀菌剂已被证明有效地减少了口服S. ut菌的增殖,但它们的重复给药引起了人们对新兴细菌耐药性和对口服微生物群的有害影响的关注。具有非致命作用机制的牙齿涂抹生物膜抑制剂为限制生物膜形成和减少对整个口腔微生物组的影响提供了一种新颖的方法。近年来,以这种身份使用纳米颗粒已引起了很大的兴趣。尽管几项研究集中在氧化元素纳米颗粒的抗菌作用上(纳米核,首席执行官2-np)很少有人专注于它们对初始生物膜形成条件下临床相关细菌的影响。在这项工作中,发现仅从CE(IV)盐(即硝酸盐铵,CAN;硫酸铵CAS)水解衍生的纳米库水解可减少体外S.在蔗糖存在下的依从性,而商业则在商业上降低了约40%“裸”纳米果(3 nm,10-20 nm,30 nm)的分散体,CE(否3)3(CN)或铵盐(AN,AS)在相似的体外条件下仅被观察到无活性或观察到生物膜形成。浮游生长和扩散测定支持生物膜生产初始阶段活跃的生物膜抑制模式。人类细胞增殖分析仅表明水解Ce(IV)盐对最高1 mm Ce的浓度的细胞代谢的较小作用,与等摩尔浓度AGNO相比,观察到的毒性较少3- 长期使用的口腔内抗菌剂。本文提出的结果在口腔医学领域具有潜在的应用。