ALS患者的脑细胞死亡,痴呆与细胞核中关键生化转运结构的丧失有关
长期以来,研究人员一直试图准确解释与肌萎缩性侧索硬化症(ALS)和额颞叶痴呆相关的最常见的基因突变是如何导致神经细胞死亡的。现在,约翰霍普金斯医学院的研究人员报告了新的证据,证明这种突变会慢慢破坏蛋白质、酶和其他物质进出细胞控制中心的重要运输系统,这一过程最终会杀死大脑和脊髓中的神经元。
研究人员表示,他们的发现于7月15日在《纽约时报》网上发表神经元确认了这一途径是开发ALS和第二大常见痴呆症新疗法的目标。估计有3万美国人患有肌萎缩性侧索硬化症,这是一种消耗性疾病,患者体内控制肌肉和运动的神经元会死亡。患有这种疾病的人会慢慢失去移动、吞咽和呼吸的能力。据估计,约有6万美国人患有额颞叶痴呆,其症状与阿尔茨海默氏症相似,会使人丧失记忆、学习能力、性格和稳定的情绪。这两种疾病都没有现成的治疗方法。基因突变C9orf72,简称C9,在约40-50%的遗传性渐冻症患者和约12%的遗传性额颞叶痴呆患者中发现。
脑科学研究所和罗伯特·帕卡德肌萎缩性侧索硬化症研究中心主任、约翰·霍普金斯大学医学院神经学教授杰弗里·罗斯坦医学博士说:“我们认为这种常见突变的工作方式就像新车上的第一个刮痕,如果时间长了,整个汽车都会生锈,直到无法工作。”
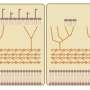
罗斯坦实验室过去的研究表明,许多神经退行性疾病(包括渐冻症)的一个共同机制是酶、RNA和蛋白质进出神经细胞核(包含遗传密码的控制中心)的运输中断。当这种传输被阻断时,神经元就会随着时间的推移而死亡。这些小分子通过细胞核中的数千个孔移动,称为核孔复合物,每一种都由30种不同的蛋白质组成,称为核孔蛋白。
为了进一步了解这一过程,由罗斯坦实验室博士后研究员Alyssa Coyne博士领导的这项新研究在30种核孔蛋白中的23种上添加了微小的化学标签,这使他们能够使用超分辨率显微镜看到核核的孔隙。
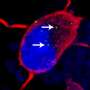
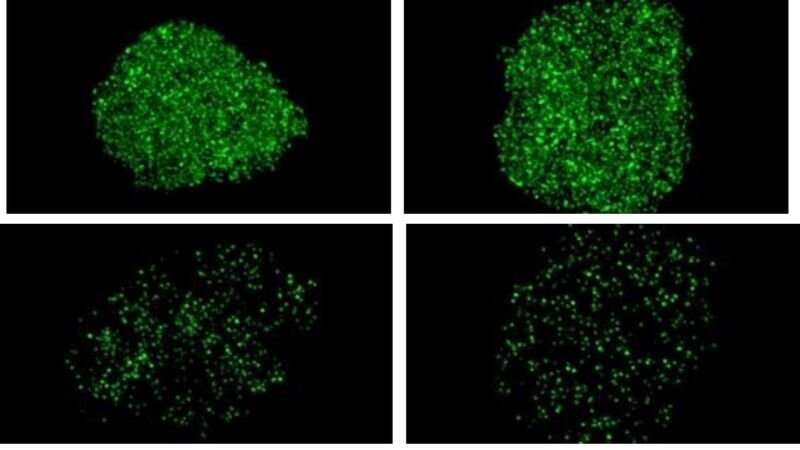
然后他们比较了孔隙健康神经元与患有导致ALS/痴呆的C9突变的人的神经元之间的交流。研究人员说,在C9神经元中,他们一直看到低水平的8种不同的核孔蛋白,这表明孔中缺少这些核孔蛋白“碎片”,导致后者细胞的运输路线中断。
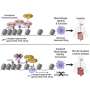
利用细胞工程的标准工具,研究人员将8个核孔蛋白基因中的每一个都加回来,以产生更高水平的核孔蛋白,从而“重建”了具有ALS/痴呆引起突变的C9细胞中的孔。他们发现,添加编码Pom121核孔蛋白的基因也能恢复所有其他7种核孔蛋白的水平,并恢复细胞物质进出细胞核的运输。
“通常情况下,当你让C9神经元受到压力时,它们会死亡。然而,当我们补充缺失的Pom121时,孔被‘重建’了,C9神经元在受到压力时没有死亡,”罗斯坦说。据研究人员介绍,Pom121是一种连接核孔内外环并将其固定在核膜上的结构蛋白。
C9 ALS/痴呆突变是如何导致核孔损伤的?C9 ALS/痴呆突变是由DNA字母GGGGCC中的重复序列引起的。这个DNA序列转化为RNA,使RNA“重复”,这是一个异常的过程,它向几个不同的蛋白质发出指令,这些蛋白质也有重复的蛋白质序列。罗斯坦指出,研究人员还不确定是RNA重复还是蛋白质重复导致了疾病的后期进展。
为了研究RNA或蛋白质在C9 ALS/痴呆引起突变的神经元中重复是否会导致核孔破裂,研究人员检查了一种去除了整个C9orf72 DNA序列的神经元。没有这个DNA序列,神经元就不能自己制造RNA或蛋白质重复。然后,他们加入了蛋白质重复序列的各种组合,尽管这些蛋白质重复序列在细胞中聚集,但他们发现蛋白质重复序列并不影响核oporin蛋白质的水平。另外,他们在这些没有C9 DNA的神经元中添加了RNA重复序列,并发现了与C9 DNA中相同的减少的核孔蛋白神经元患有C9突变的渐冻症/痴呆症患者。
“这一发现证实,针对C9突变人群RNA重复的药物可能是治疗ALS或ALS患者的一种方法额颞叶痴呆通过干扰‘生锈’过程,”科因说。“有希望的是,临床试验中有几种药物可以通过与RNA重复序列结合并将其分解来治疗ALS。”