研究人员对小鼠克拉斯突变体肺肿瘤进行了有效的策略
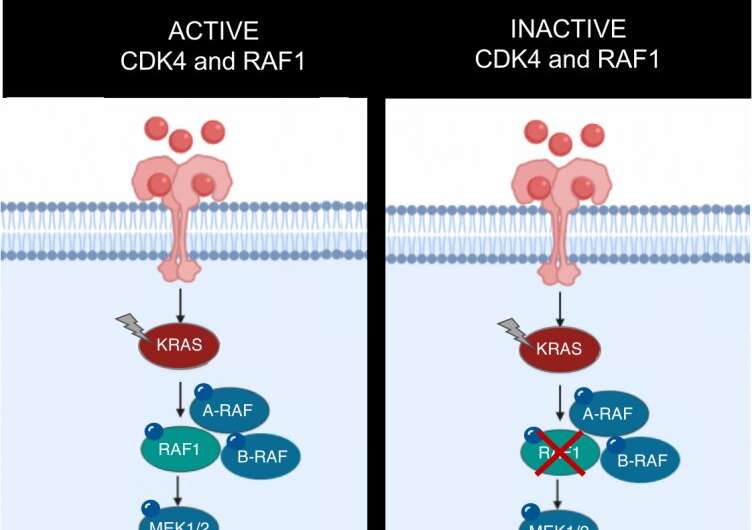
KRAS致癌基因参与了至少五分之一的人类癌症:KRAS突变直接导致了32%的肺肿瘤和96%的胰腺肿瘤。然而,经过三十多年的研究至今,仍然没有针对这种致癌基因的有效治疗策略。因此,许多研究试图识别KRAS信号通路上显示治疗活性的其他分子。为了应对这一挑战,西班牙国家癌症研究中心(CNIO)实验肿瘤小组的研究人员在CDK4和RAF1基因灭活后,该致癌基因在小鼠中诱导的25%的肺肿瘤得到完全缓解,这为未来治疗的发展开辟了新的场所。这一发现已由PNAS这是美国科学院的期刊。
在这个项目中,CNIO团队探索了一种包括灭活KRAS信号通路的两个基因:CDK4和RAF1的方法。这项研究的主要作者之一Monica Musteanu说:“这个策略确实奏效了。”通过研究小鼠模型肺癌由两种突变的组合引起的kras癌基因的激活和消除肿瘤抑制基因p53,人类癌症中的两个最常见的突变基因 - 它们已经设法缩小了100%的肿瘤,其中四分之一有四分之一完全汇款。此外,研究人员在健康的小鼠中证实,这种治疗策略不会损害身体正常功能。
即便如此,正如经常发现的临床实践在没有CDK4和RAF1的情况下,一定比例的肿瘤能够存活。然而,研究人员能够识别分子机制引发这种抗性并防止总肿瘤缓解:激活PI3K途径,癌症必需品,以及通过甲基化沉默几种肿瘤抑制基因。“这两种机制都可以治疗:使用PI3K抑制剂,一方面,通过肿瘤抑制基因的选择性去甲基化重新激活其功能,”Laura de Esteban解释说,该研究的主要作者发表PNAS。
为了开展这项研究,CNIO团队使用了一种鼠标模型这准确地再现了人类疾病这是一种通过激活KRAS致癌基因和使p53抑癌基因失活来诱导侵袭性肺肿瘤的基因组合,这种基因组合在人类肺腺癌中占很大比例。然后,一旦肿瘤形成,老鼠体内的基因就会被系统地灭活,就像病人在确诊后接受治疗一样。
这些发现揭示了KRAS突变肿瘤新疗法的发展,并指出了开发针对RAF1的抑制剂的重要性,因为由于其高毒性,迄今为止开发的抑制剂还没有通过第一阶段。
此外,作者还指出,未来的另一个研究领域将是在治疗靶标失活可能出现的多种抗性途径的研究。
进一步探索











用户评论