制药公司负责人誓言在疫苗竞赛中绝不“偷工减料”
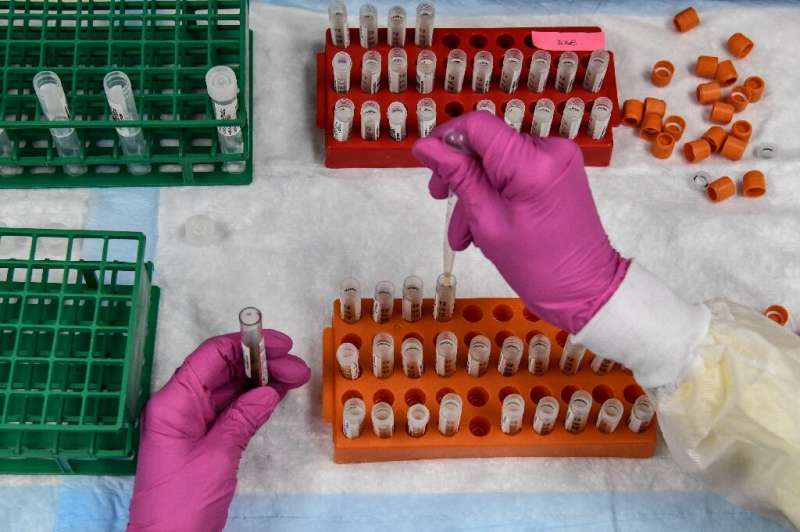
制药公司高管周四坚称,他们不会试图将不符合严格安全和效率标准的Covid-19疫苗或治疗方法推向市场。
世界各地的政府都希望宣布疫苗尽快开始对小说进行治疗冠状病毒该病毒已造成86万多人死亡,超过2600万人感染。
但这种紧迫感让人担心,公司和监管机构可能会匆忙进行试验,以确保疫苗或治疗方法可以安全使用,并真正有效地对抗这种疾病。
"我们不会偷工减料,"辉瑞首席执行官Albert Bourla在虚拟新闻发布会上对记者表示。
辉瑞及其合作伙伴bioontech希望最早在下个月完成新冠肺炎候选疫苗的最后阶段三期试验。
在国际制药制造商和协会联合会(IFPMA)主办的简报会上,其他几位制药公司高管也承诺,在申请批准新冠病毒疫苗或治疗方法之前,要坚持严格的安全和效率标准。
“不会牺牲安全”
礼来公司负责人Dave Ricks表示,在将此类产品提交监管机构之前,“我们首先要达到自己的安全性和有效性标准,这是很高的标准。”

“我们不会在任何情况下牺牲安全,”默克首席执行官肯尼思•弗雷泽(Kenneth Frazier)表示赞同。
就在他们发表上述言论的前一天,有消息称华盛顿敦促美国各州为可能在11月1日之前推出的Covid-19疫苗做好准备,这引发了人们对唐纳德·特朗普政府急于在11月3日大选前开始分发疫苗的担忧。
在正常程序下,试验管理人员必须等待数月或数年才能验证候选疫苗的有效性和安全性。
然而,美国食品和药物管理局(fda)提出了一种可能性,即在试验结束前,一种疫苗可能获得紧急授权。
FDA面临着来自医疗界的指控,称其是在屈从,但FDA否认了这些指控政治压力特朗普在民调中落后于民主党挑战者乔·拜登。
“我也理解他们持怀疑态度……因为现在有太多的科学政治化了,”辉瑞首席执行官Bourla说。
但他强调,“在我们觉得疫苗安全和有效之前,我们绝不会自己提交授权或批准。”
Bourla告诉记者,已经有超过2.3万人参加了试验,主要分布在美国和巴西的125个地点,这些公司预计在“几天内”就能达到必要的3万名参与者。
他希望到10月底“能够有足够多的活动来说明该计划是否有效。”
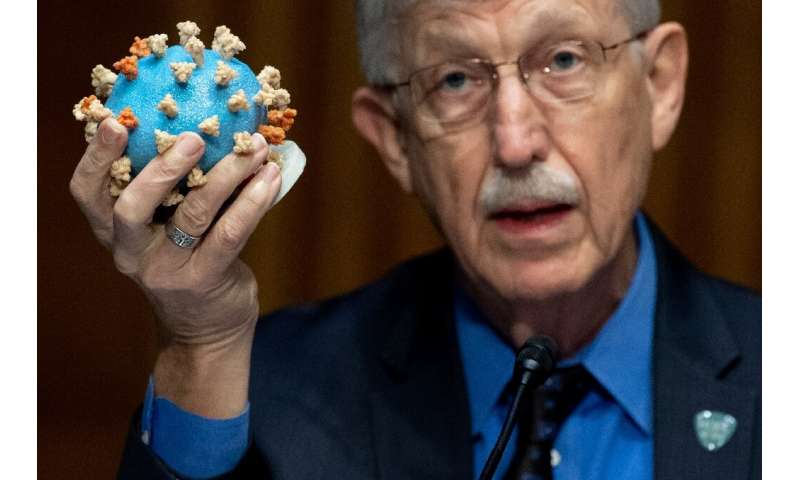
“非常彻底的过程”
吉利德首席执行官丹尼尔•奥戴(Daniel O’day)坚称,获得紧急使用授权的过程并非易事,他指出,吉利德的抗病毒药物瑞德西韦(remdesivir)获得紧急使用授权的经验已被证明对治疗Covid-19有效。
他说:“这是一个非常彻底的过程。
罗氏首席执行官塞维林•施万(Severin Schwan)表示,该行业已表明了对数据透明度的承诺,并致力于保持较高的检测标准,尽管在结果方面面临压力。
他指出,他的公司令人失望的发现,其关节炎药物tocilizumab(以actemra的品牌名出售)本身并不是一种药物有效的治疗正如坊间证据所表明的那样。
“我们不可能降低进行试验的标准,”他说,并补充说,Actemra试验“证明了这一点”。
罗氏仍在测试Actemra与其他药物(包括吉利德的瑞德西韦)合用时是否有效。
©2020 AFP











用户评论