1型糖尿病:单宁酸包封保护移植胰岛免受排斥
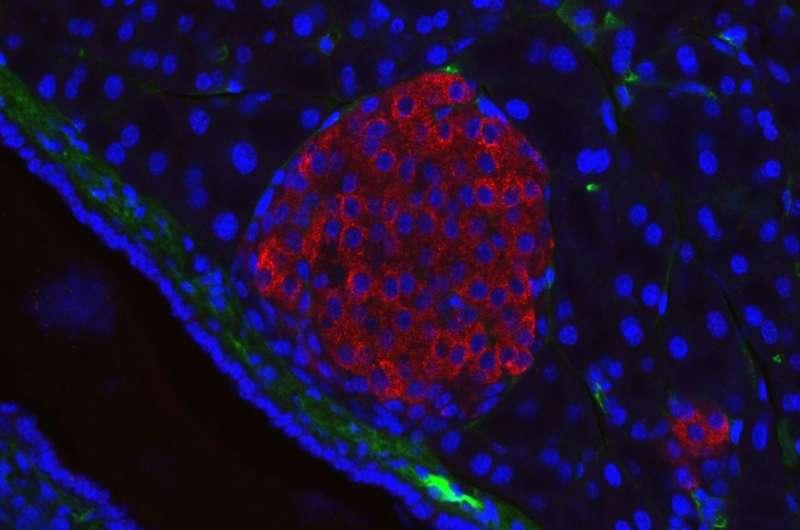
1型糖尿病,简称T1D,是由胰腺中产生胰岛素的细胞自身免疫性破坏引起的。患有T1D的人需要外源性胰岛素,血液中葡萄糖水平的波动会影响预期寿命,并增加心血管疾病、神经疾病和肾衰竭的风险。
一种疗法很有前途——移植胰腺胰岛从尸体。但这需要免疫抑制,重新激活的自身免疫会导致移植物在五年后存活能力和功能低下。
现在,阿拉巴马大学伯明翰分校的一组研究人员展示了一种保护移植胰岛的简单方法,即在胰岛上涂上一层由两种生物聚合物交替层组成的薄皮肤。正如杂志报道的那样糖尿病在T1D小鼠模型中,这种涂层延缓了同种异体移植和自身免疫介导的排斥反应。
“我们的方法是用聚(n -乙烯基吡咯烷酮)-抑制促炎免疫反应丹宁酸-包膜胰岛而无全身免疫抑制是迈向成功的重大进展胰岛资深作者Hubert Tse博士和Eugenia Kharlampieva博士说。
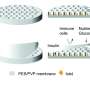
生物相容性的聚(n -乙烯基吡咯烷酮)-单宁酸,或PVPON和单宁酸,或TA,被涂在胰岛上的多层交替层,足够薄,可以让氧气和营养物质轻松到达细胞。这种纳米薄的胶囊大约比保鲜膜薄120倍。UAB的研究人员说,其自身免疫保护的关键是TA层。这种酚类化合物可以清除活性氧还有消炎的功效。
我们已经知道,来自活性氧(ROS)的氧化应激在激活移植胰岛的异源反应性和自身反应性免疫中起着关键作用,而且胰岛产生胰岛素的β细胞比身体的许多其他细胞对ROS更敏感。
在UAB研究的自身免疫移植实验中,超过一半的(PVPON/TA)包裹的移植物在移植后70天存活,而不到四分之一的未包裹的移植物存活。在同种免疫移植实验中,胰岛来自不同品系的小鼠,大约40%的包膜移植物在移植后120天存活,而所有未包膜移植物在不到50天内就发生排斥反应。
在两种类型的移植中,均不存在全身性免疫抑制。(PVPON/TA)包封的胰岛维持正糖状态的时间明显长于未包封的胰岛,移植物具有免疫调节作用。
与未包膜的小鼠相比,接受包膜移植的小鼠免疫细胞浸润、ROS合成、炎症趋化因子、细胞因子和CD8 T细胞浸润显著降低。ROS可促进促炎M1巨噬细胞分化;相比之下,接受包膜胰岛的小鼠抗炎M2巨噬细胞增加。
Tse和Kharlampieva说,可以做更多的工作来改善免疫抑制,并将这种保护扩展到比人体尸体胰岛更容易获得的其他胰岛来源。
他们说:“PVPON/TA涂层可以被修饰以增加PVPON和TA被囊层数,与免疫抑制受体(包括CTLA-4、PD-L1和/或抗炎细胞因子,如IL-10和tgf - β)复合,以进一步增强局部免疫抑制。”“PVPON/TA涂层的使用不仅限于人类胰岛的包封,因为我们的初步研究还表明,PVPON/TA包封不会损害新生儿猪胰岛的功能,而且还可以扩展到包括人类干细胞来源的胰腺β细胞。”
进一步探索












用户评论