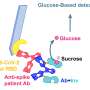
辉瑞公司BioNTech寻求紧急COVID-19镜头在美国的使用

辉瑞正式要求美国监管机构周五允许紧急COVID-19疫苗的使用,启动时钟这一过程可能带来有限的第一枪最早在下个月,最终结束但是直到经过漫长,艰难的冬天。
行动几天前,辉瑞公司和德国合作伙伴BioNTech宣布,其疫苗出现95%有效防止轻微到严重COVID-19疾病在一个大的,正在进行的研究。
公司说,保护+良好的安全记录意味着疫苗应符合紧急使用授权,美国食品和药物管理局可以授予前的最后测试是完全完成。除了FDA提交,他们已经开始“滚动”应用程序在欧洲和英国和打算尽快提交类似的信息。
与美国和全球激增的冠状病毒,监管机构的压力做出快速的决定。
“帮助,”Anthony Fauci博士,美国传染病专家说辉瑞的前夕宣布,并称还为时过早放弃面具等防护措施。“我们需要兼任公共卫生措施为我们等待帮助。”
周五申请引发一连串的事件作为FDA和独立顾问讨论如果照片准备好了。如果是这样,还是另一个政府组织必须决定如何最初的有限供应限量供应焦急地等待美国人。
有多少疫苗可用,当一个移动的目标,但最初将稀缺和定量供应。在全球范围内,辉瑞公司估计到今年年底可能会提供5000万剂量。
2500万12月可能成为美国可供使用,3000万年1月和3500万年2月和3月,根据国家科学院医学信息提交给这个星期。收件人需要两剂,三个星期。美国政府合同购买数百万Pfizer-BioNTech剂量,比结果以及其他候选人,并许诺将是免费的。
不是远远落后于竞争对手现代化Inc .) COVID-19疫苗。早期数据显示,如辉瑞的镜头,这公司还预计将在数周内寻求紧急授权。
接下来会发生什么:
公开的数据
公众的第一次有机会看到强大的证据确实是会12月10日的公开会议上FDA的科学顾问。

到目前为止,已知的是只基于从辉瑞和BioNTech语句。170感染检测到目前为止,只有八等人收到实际的疫苗和其他已经假枪。在安全方面,公司引用的结果从38000名研究参与者已经跟踪了两个月后他们的第二个剂量。这是FDA设定一个里程碑,因为从历史上看,疫苗的副作用比这晚不出现。
“这些数据,我们将深入”FDA顾问Paul Offit博士说费城儿童医院的。
把它像科幻受审。前几天开会,FDA将发布自己的内部分析。奠定了基础的顾问一整天的讨论任何安全问题的迹象,新疫苗技术是如何工作之前呈现裁决。
不仅他们会建议FDA是否应该允许广泛使用的疫苗一般,但如果是这样,为谁。例如,是否有足够的疫苗证明是好老,病情加重的成年人对于年轻,健康的人?
仍然没有保证。“我们不知道这是投票,”FDA疫苗前首席诺曼·贝勒说。
紧急使用不一样的全部批准
如果有紧急的绿光,“疫苗仍被视为临床实验。还没有批准,”马里恩博士格鲁伯,FDA局长疫苗办公室本周告诉《国家科学院医学。
这意味着任何人提供紧急疫苗接种必须得到一个“简报”描述之前经历的潜在益处和风险的,她说。
将会有很多的未知数。例如,95%的保护是基于然后出现症状的人进行病毒检测。可以接种感染,但没有任何症状,能够传播病毒吗?保护持续多长时间?
这就是为什么44000人的研究中需要继续运营困难的考虑道德,参与者给假照片在某种程度上必须提供真实的疫苗,使寻找答案。
说:“我很好奇,巴里·科尔文,52岁,白色的平原,纽约,参加纽约大学Langone健康研究。
但他并不是一个伟大的急于找出哪一组他。“你需要坚持一段时间理解和回答的很多其他问题仍然未知。”

另外至少在目前,孕妇不会有资格,因为他们没有研究。辉瑞公司最近才开始测试疫苗的孩子12。
决定Pfizer-BioNTech疫苗不会影响其他COVID-19候选疫苗的管道,将分别评价。
制造业
酿造疫苗比典型的药品生产更复杂,然而,一百万剂量推出辉瑞的卡拉马祖,密歇根州,工厂必须相同的纯度和效力每个剂量之前和之后。
这意味着FDA的决定并不是基于研究数据,但其决心,疫苗是正确的。
的Pfizer-BioNTech疫苗和现代化的拍摄是由全新的技术。他们不包含实际的冠状病毒。相反,他们用一块“飙升”蛋白质的基因编码钉病毒。
信使RNA或信使RNA,指示身体做一些无害的蛋白质,训练免疫细胞识别它最终如果真正的病毒。
进入人的怀里
另一个政府group-advisers疾病控制中心和Prevention-decides谁成为了稀缺的剂量。卫生与公众服务部长亚历克斯Azar说他希望可以做出决定的同时,美国食品和药物管理局。
特朗普政府操作翘曲速度曾与国家排队他们需要多少剂量覆盖人群提供疫苗。
辉瑞将仅限于船舶供应有序的FDA给好。
船公司的预测是多少每个月只是预测,贝勒警告说。
“这不是像一个披萨,”他说。制造业是这么复杂,“你不一定得到你想。”
进一步探索
©2020美联社。保留所有权利。材料可能不会被出版,广播,重写或重新分配。